



一代PARP1抑制剂能靶向PARP1/PAPR2,为非选择性抑制剂,目前已有多款药物先后上市,如Olaparib(Merck/AZ)、Niraparib(GSK/Zai lab)、Rucaparib(Clovis)、Talazoparib(Pfizer/Medivation)、氟唑帕利(恒瑞)、帕米帕利(百济)等。这类药物在卵巢癌、乳腺癌、前列腺癌等适应症上获得成功,证明了PARP1/PAPR2是极具价值的合成致死药物靶点,但其脱靶效应所导致的安全性风险,如贫血、血小板减少、中性粒细胞减少等限制了使用。以阿斯利康AZD5305为首的选择性靶向PARP1抑制剂目前正在临床研究阶段,已显示出更好的靶向性和安全性,以及富有吸引力的药效学结果。
本文将针对文献所披露的一代、二代PARP1抑制剂的相关资料进行分析,并结合熙宁生物|精翰生物二代PARP1抑制剂的临床药效学评估实践,对合成致死靶点临床药效学评估的逻辑进行系统性介绍。
PART 01
一代PARP1临床药效学评估方法学
双链DNA断裂(DSB)会导致PARP1被招募到有缺口的DNA,并被迅速激活,导致包括其自身在内的多种蛋白发生PARylation修饰,从而启动DNA修复机制。双链断裂(DSB)修复缺陷的癌细胞,如BRCA1/2突变细胞,基于“合成致死”的机理,对PARP1抑制剂格外敏感。
PARP1抑制剂可以抑制PARP1活性,会导致双链DNA修复信号通路多种蛋白的PARylation修饰减少。基于药物作用原理,检测用药前后患者PBMC中PAR(Poly ADP-ribose)的水平是一代PARP1临床药效学评估的经典技术路径。相关文献披露了两种检测方法以及一种改良方法:

方法一:体外刺激酶催化反应检测方法
Rucaparib (AG014699)采用体外酶催化反应检测方法,将用药后的人PBMC加入NAD+ 和oligonucleotide进行体外刺激酶催化反应,将反应后的产物使用western blot进行半定量检测。


方法二:PBMC裂解ELISA检测方法
Veliparib采用的是分离用药前后的PBMC细胞,在裂解PBMC变性蛋白后,使用ELISA对PAR进行定量检测。依据的方法为NIH公开披露的经验证的PAR检测免疫学方法。



方法三:辐照后PBMC裂解ELISA检测方法
鉴于方法二对ELISA检测PAR的灵敏度要求较高,Rosemarie de Haan等建立了新的方法,即在用药前后的PBMC中加入有药物的血浆进行辐照,然后再进行PBMC分离裂解,待PBMC蛋白变性后,使用ELISA对PAR进行定量检测。


三种方法学要素比较:
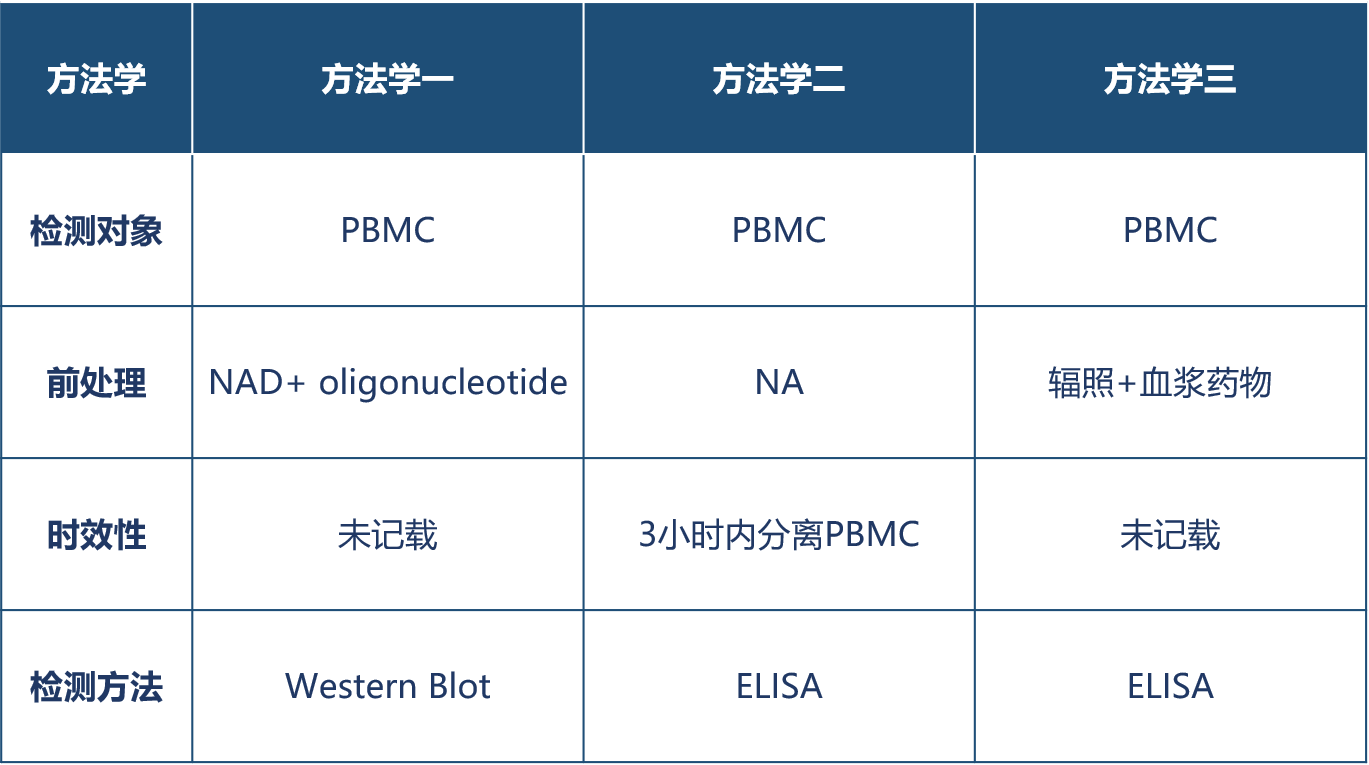

三种方法学的优劣比较:
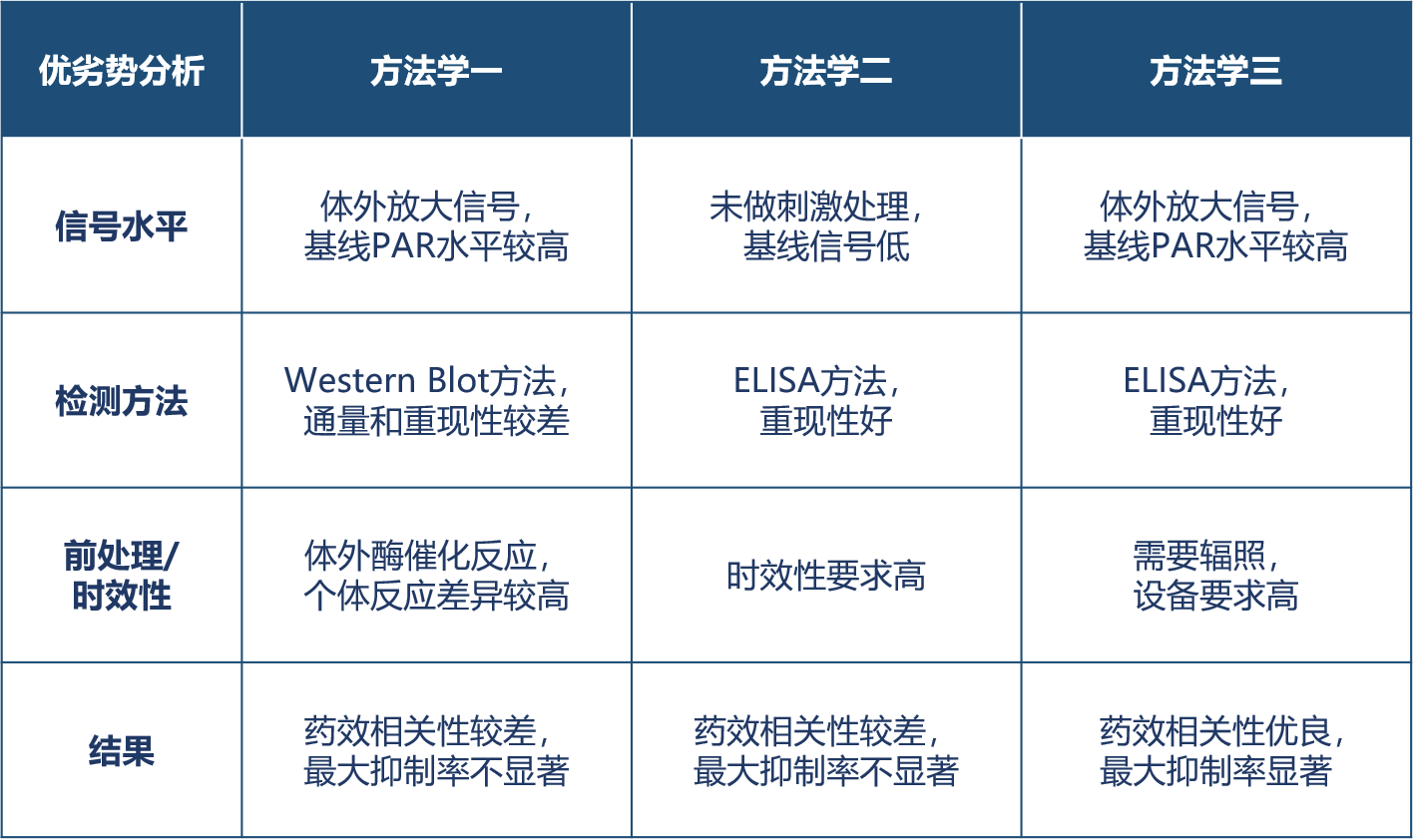
总结下来,一代PARP1抑制剂的PD方法学,因为样品时效性要求、PBMC需要体外反应、方法学灵敏度要求高、仪器设备可及性等原因,要做出药物和PAR水平的显著性药效相关性难度较高,方法学稳固性和重现性较差。
PART 02
二代PARP1临床药效学评估方法学
AZD VS 熙宁|精翰

AZD5305方法学:
体外刺激酶催化反应MSD检测方法
创新的药物需要有适配的创新型临床药效学PD方法来进行表征,AZD5305披露的PARP1的数据中,20mg剂量组有66.7%受试者能达到90%抑制率,60mg剂量组有84.6%试者能达到90%抑制率,较之前的一代PARP1抑制剂对PAR抑制作用有极为显著的提升。

AZD5035如此优秀的PD数据,除了药物本身的药效作用外,从方法学角度来说,该创新型的方法学进行了前处理,放大了信号值,同时利用新的MSD方法降低了检测下限,这是最大抑制率能够达到90%以上的关键。


熙宁|精翰PARP1药效方法学:
全血体外损伤刺激全新ELISA检测方法
熙宁生物|精翰生物基于一代PARP1药效学方法的经验,以及AZD药效方法学在实际临床生物分析过程中可能会遇到的问题,开发了创新型的PARP1抑制剂临床药效学方法,实验体系如下:
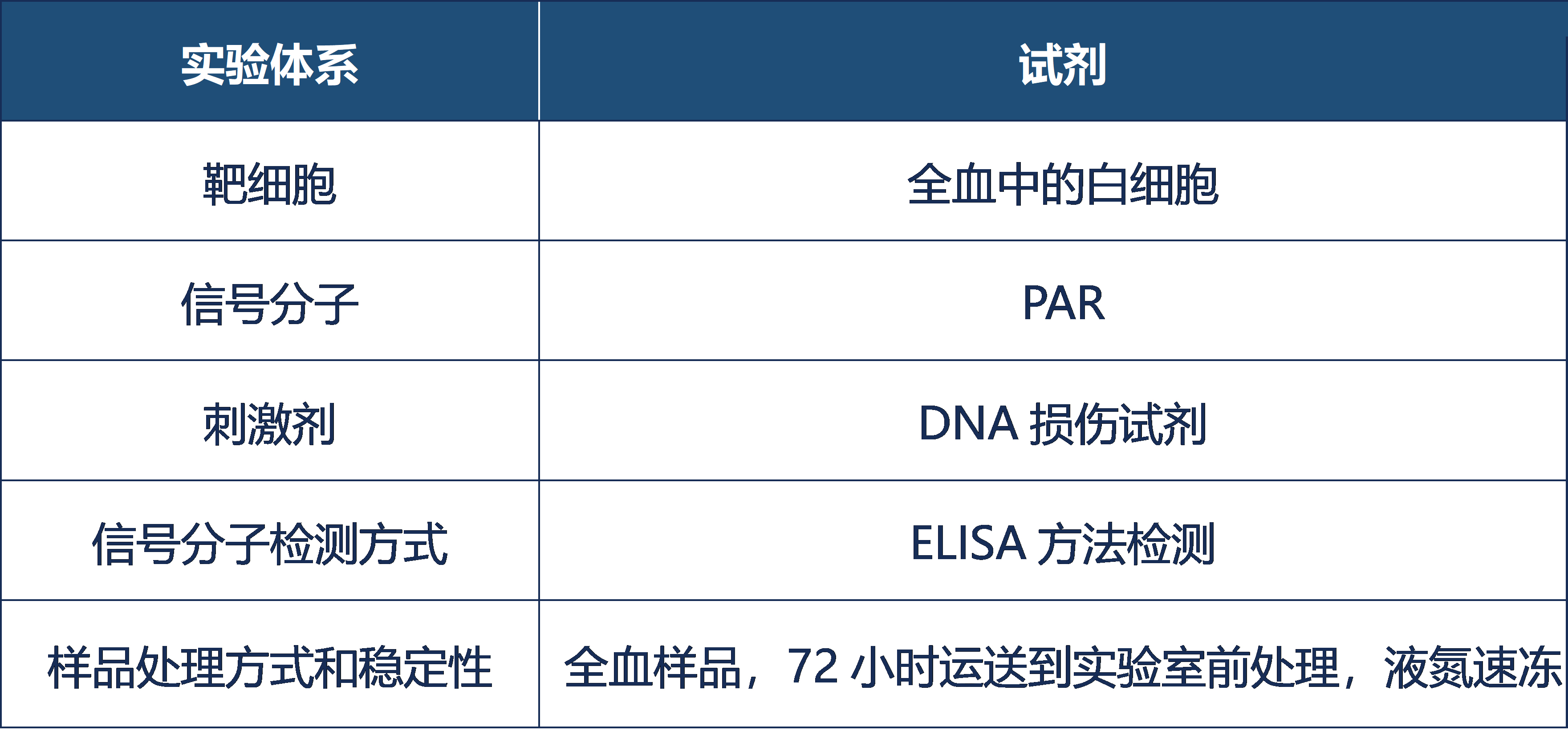
该方法学与一代PARP1的方法学三类似,进行了全血刺激前处理。同时,由于某产商的PAR检测试剂盒产品升级迭代,不适用于全血基质中PAR检测,我们重新筛选PAR抗体对,建立了高灵敏度抗干扰的ELISA检测方法。该PARP1方法学已经过全验证且成功应用于临床样品分析,取得了非常好的药效学数据。全血基质中典型的药效曲线如下:
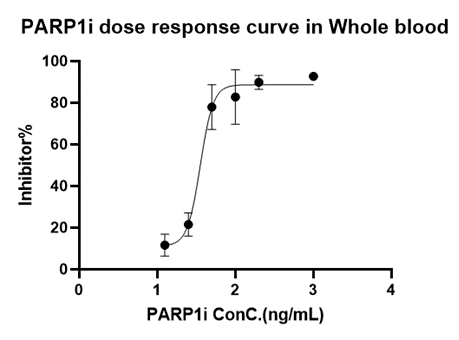
相对于AZD方法学分离PBMC后再裂解进行体外信号放大,熙宁生物|精翰生物的方法学使用全血刺激进行信号放大,保留了全血中的药物,使其持续发挥药效学作用,其生理学相关性和方法稳固性更好。
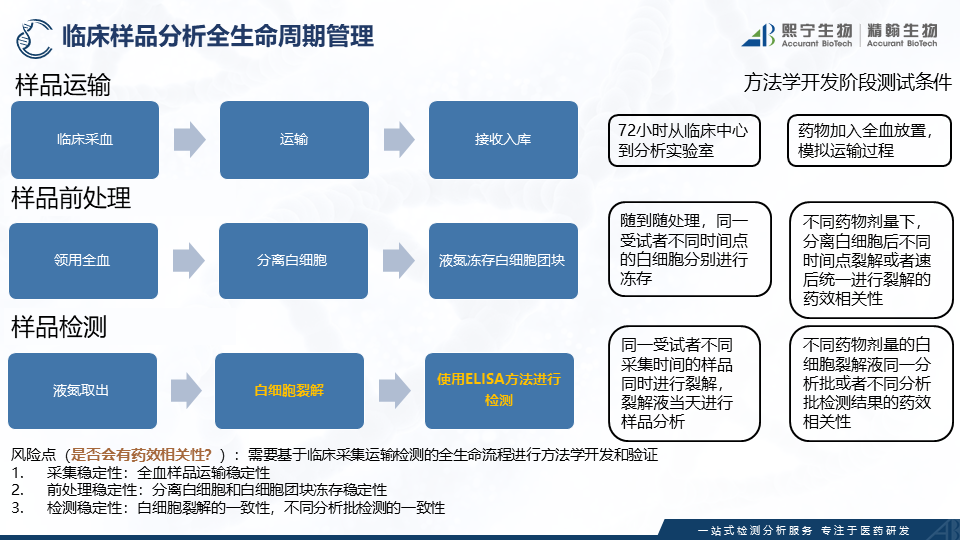
同时,对于PARP1药效学方法对于样品的时效性和结果稳定性要求,熙宁生物|精翰生物也在临床样品分析的全流程中建立了周期管理,如下图包括全血采集稳定性,白细胞冻存稳定性,白细胞裂解的操作流程等。
PART 03
熙宁生物|精翰生物的临床药效学分析和
转化医学服务
使用人来源基质进行药效学评估,可以避免动物模型的种属差异,对于人体的反应有非常好的预测性作用,在药物的成药性评估上起到了越来越重要的作用,在进行同类对标阳性药物和候选药物的药效比较中,更具有生理相关性的优势;同时对于预测候选药物和同类对标药物在临床的表现,可以提供较多的有价值信息。同时也能对药物在临床一期的起效剂量和饱和药效剂量进行预测。
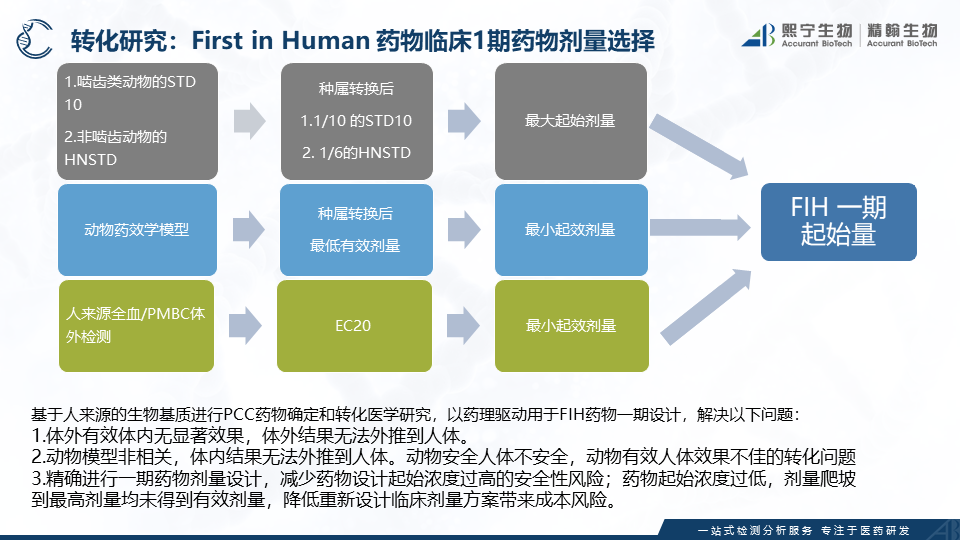
在临床一期药物药效学方法开发阶段,经过严格和充分验证的方法学,可以提供较为精密的临床一期药效学数据,对于二期药物剂量的选择也有很大的参考价值。
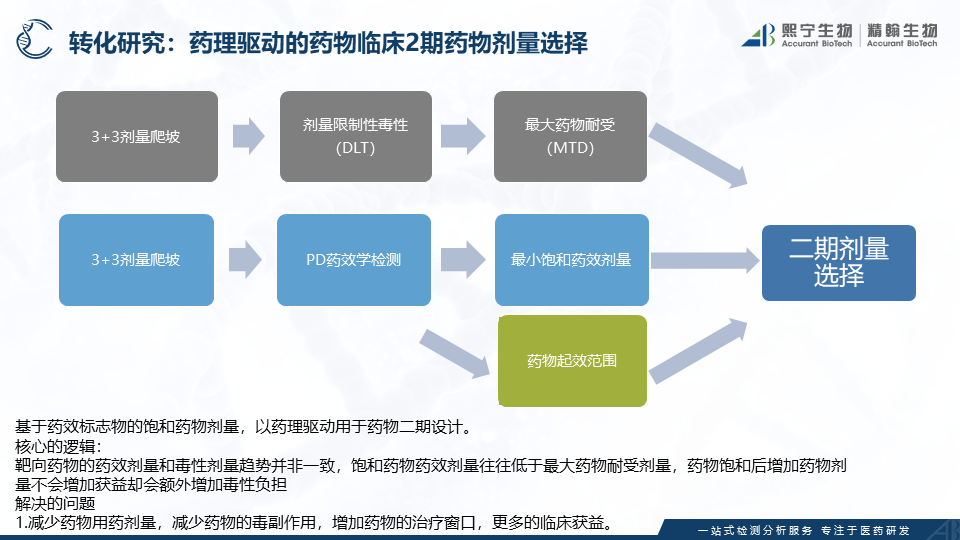
熙宁生物|精翰生物在基于人全血基质的药效学生物分析检测的方法开发,验证和样品分析方面有着丰富的经验。我们可以提供临床前和临床阶段全血基质的药效学方案设计和药效检测服务,还能够为候选药物分子的成药性评估,临床一期二期的药物剂量设计决策提供专业化的转化医学服务。欢迎后台留言咨询。
参考文献
[1] Plummer ER. etc.Temozolomide pharmacodynamics in patients with metastatic melanoma: dna damage and activity of repair enzymes O6-alkylguanine alkyltransferase and poly(ADP-ribose) polymerase-1. Clin Cancer Res. 2005 May 1;11(9):3402-9. doi: 10.1158/1078-0432.
[2] NCI DoCTaD. [cited 2015 20-10-2015]; Available from:.
[3] de Haan R, etc. Improved pharmacodynamic (PD) assessment of low dose PARP inhibitor PD activity for radiotherapy and chemotherapy combination trials. Radiother Oncol. 2018 Mar;126(3):443-449. doi: 10.1016/j.radonc.2017.10.017. Epub 2017 Nov 14. PMID: 29150161.
[4] Benedetta Lombardi, etc; Abstract CT269: A highly sensitive and specific PARylation assay confirms significant and durable target engagement by AZD5305 in patients. Cancer Res 15 April 2023; 83 (8_Supplement): CT269. https://doi.org/10.1158/1538-7445.AM2023-CT269
[5] Skånland, S.S., Tjønnfjord, G.E. Determining drug dose in the era of targeted therapies: playing it (un)safe?. Blood Cancer J. 12, 123 (2022). https://doi.org/10.1038/s41408-022-00720-7