



第一件事:质谱可以检测蛋白类药物吗?
随着蛋白类药物研发的快速发展,其检测需求也日趋增多。免疫分析法是检测该类药物的常规方法,其具有灵敏度高和专属性强等优点,但也存在一定的局限性,比如相对较窄的线性范围,方法精密度和重现性相对不佳,以及较大的基质干扰,这些在一定程度上影响了蛋白类药物检测的准确性。由于蛋白类药物分子量远远超过质谱分析仪器的质荷比检测上限,因此不能直接对该类药物进行检测。目前常规方法主要是通过将蛋白类药物变性、还原、烷基化,然后使用蛋白酶裂解,形成特征性的肽段,这些肽段具有良好的色谱和电离特性,几乎无复杂的氨基酸残基或修饰,能够呈现线性和精确的响应。
第二件事:哪些蛋白类药物可以使用质谱检测?
蛋白质的基本结构单元是氨基酸,构成天然蛋白质的氨基酸有20多种。蛋白质结构中化学键包括共价键与非共价键,共价键有肽键和二硫键,非共价键有氢键、疏水键、离子键、范德华力与配位键等。蛋白质的结构可分为一、二、三、四级结构,一级结构为初级结构,二、三、四级结构为高级结构或空间结构。蛋白质的化学降解与温度、pH值、离子强度和氧化剂的存在等密切相关,也与蛋白质的结构与性质有关。蛋白类药物主要分为四类:
第一类:应用蛋白质的酶活性及调节活性进行治疗的蛋白质药物。该类药物多为功能活性明确、作用位点清楚的蛋白分子。目前已经上市的非抗体类重组 蛋白质药物均属于此 类,可 细 分 为 以 下3组:
a)替代缺乏或异常的蛋白质:因为许多疾病是由于特定的蛋白缺乏或异常引起的。本组药物通过持续给予该蛋白,治疗由确定的分子病因学造成的内分泌及代谢性疾病,如治疗由于激素缺乏的胰岛素、生长激素等。
b)增强蛋白质生物活性通路的药物:主要通过增强血液或内分泌通路或增强免疫反应来达到治疗作用。本组药物主要为人体 内正常情况下存在的细胞因子、内分泌激素、凝血酶类分子或它们的类似物等,具有微量强效、作用快速等特点。
c)提供新功能或新活性的蛋白药物:使用天然存在的蛋白质来治疗人类病理生理学疾病,如对大分子酶促降解的胶原酶、透明质酸酶和阿法链道酶,对小分子代谢物酶促降解的PEG修饰。
第二类:有特殊靶向活性的蛋白质治疗药物。本类药物以单克隆抗体、免疫球蛋白相关分子为主。
a)直接干扰靶分子或靶组织功能的蛋白。主要是各种治疗性抗体,如利妥昔单抗、曲妥珠单抗、贝伐单抗、英夫利昔单抗、阿达木单抗等。
b)传递其他化合物的药物:该类药物利用蛋白质可特异性结合治疗靶点的能力,借助蛋白质为传输载体,将高毒性的小分子药物、毒素或同位素等效应分子靶向运送至疾病部位 从 而 发 挥 治 疗作用。
第三类:蛋白或多肽疫苗。伴随蛋白或多肽疫苗制造技术的发展,“治疗性疫苗”的理论及应用不断成熟,从本质上改变了传统疫苗的概念。无论从研发手段、生产工艺,还是从产品标准、质量控制等角度,蛋白或多肽疫苗与蛋白质药物已经没有区别。因此将蛋白或多肽疫苗归为蛋白质药物范畴是一种必然趋势。
第四类:用于诊断的重组蛋白质药物。该类重组蛋白质药物兼有药物及诊断试剂的双重功能,可用于某些特定疾病的体外及体内诊断,如肿瘤显像剂多用抗体偶联同位素,在肿瘤 定位诊断的同时,同位素也可能对瘤细胞发挥抑制或杀伤作用。
第三件事:与传统配体结合方法(Ligand binding assay ,LBA)比较,质谱技术有哪些优势?
经典的蛋白质药物定量分析采用LBA技术,其中以酶联免疫吸附实验法(Enzyme-linked immunosorbent assay, ELISA)为代表,该技术的主要优点是对仪器设备要求低、易于操 作以及灵敏度高。但是也存在一定的缺点,例如:方法建立时间长、受内源性抗体的干扰、定量范围窄、非特异性结合以及交叉免疫等。近年来备受关注的质谱技术,在蛋白药物定量分析中,具有良好的选择性、准确性、精确性、定量范围宽、开发时间短(约几周时间)、分析通量高以及多重分析能力的优点。与 LBA方法相比,质谱技术的优点主要体现在以下几点:
第一,质谱方法开发的步骤包括质谱和液相方法的建立、样品的前处理、方法学验证,这些步骤耗时短,一般只需要2-4周,耗费成本也低。相反,LBA方法开发的步骤包括关键试剂的优化、内源性干扰物质的检查、不同来源样品的交叉验证。建立LBA方法需要开发关键试剂,要耗费大量的时间,而且耗费成本较高。
第二,质谱方法使用同位素标记的肽段或蛋白质作为内标,可以有效地校正分析过程中的偏差和基质效应。只要正确的维护仪器和执行相关的质量控制标准,质谱方法是非常稳定,而LBA的关键试剂都是通过生物过程产生的,容易受到蛋白质翻译后修饰等因素的 干扰,而且LBA方法难以使用内标来纠正定量偏差,很难保持较高的批间/实验室间的一致性。
第三,质谱方法通过色谱分离和同位素标记内标物的校正可以最大程度地降低基质效应的影响,并且能够适用于不同的生物基质,因此可以同时开发出应用于不同组织和器官的方法,用以定量其中药物浓度。相反,LBA方法很难应用在不同的基质(血浆或组织)以及不同的物种之间,不同的基质成分引起的干扰和交叉反应非常明显,对LBA的特异性有很大的影响。
最后,质谱可以同时检测多个待测物,特异性强,能很好的避免基质干扰,特别适用于一些受到内源干扰很强的项目,此外,还拥有较宽的线性范围。而LBA一般很难同时检测多个待测物,线性范围也相对较窄,也易受到内源干扰的影响。
第四件事:质谱检测蛋白类药物的一般步骤有哪些?
如图1所示,目前常规的方法主要是通过将蛋白类药物变性、还原、烷基化,使用蛋白酶裂解以形成特征性的肽段,最后筛选响应高、干扰低的特异性肽段进行检测。由于蛋白类药物多重的空间结构,需要进行打开空间结构。常见的变性方式主要有高温、添加有机试剂、强酸、盐类以及其他的蛋白质变性剂。此处特别注意添加变性剂对于后续蛋白酶活性的影响。蛋白类药物结构中含有二硫键,需要打开二硫键和保护巯基避免二聚体形成。常规的还原试剂包括DTT和TCEP,烷基化试剂包括碘乙酰胺。这里需要关注反应条件(pH和温度)。酶解过程是蛋白质药物检测最关键的步骤,大部分药物都可以使用胰蛋白酶进行酶解,主要作用赖氨酸和精氨酸的羧基端。酶解产生很多片段我们需要同蛋白质数据库进行比对,筛选出特异性片段,一般选择可变区域的片段作为候选肽段。
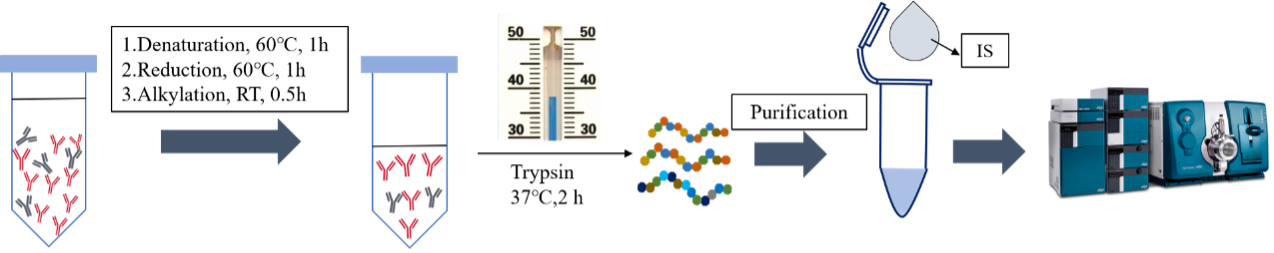
图1
第五件事:有质谱检测蛋白类药物成功的案例?
目前熙宁生物质谱平台基于LC-MS已开发出检测英夫利西单抗、新冠中和抗体、帕博利珠单抗等蛋白质类药物的方法,并成功应用临床样品检测。实验数据表明,质谱检测蛋白类药物拥有非常高的精密度、准确度和重现性,且临床试验样品再分析(ISR)结果高达99%以上,体现出特别出色的方法可靠性。
结束语
熙宁生物质谱平台能够提供符合NMPA/FDA/OECD/EMA的各项生物样品分析服务,支持小分子药物、多肽、寡核苷酸、PROTAC、ADC以及大分子抗体等药物的方法开发、验证和样品检测。平台配备了多套高端液质联用系统和Watson LIMS在内的生物分析系统和软件系统,各种先进辅助设备,不仅可以满足各型实验的检测需求,还大大提高实验效率和质量,更高效地帮助客户完成药品研发。
参考文献:
1. Fu Wei, Chen Qian, An Bo. Qualitative and quantitative characterization of protein biotherapeutics with liquid chromatography mass spectrometry[J]. Chin Hosp Pharm. 2019 Aug;39(16):1703-1708.