



溶瘤病毒治疗(oncolytic virus,OV)作为肿瘤免疫治疗的一种方法,主要通过激活机体自身免疫系统和裂解肿瘤细胞来发挥作用。近年来,随着研究的不断深入、技术的不断发展和指导原则的持续规范,研究者们不断提高溶瘤病毒对肿瘤的靶向性,降低其对正常细胞的影响,提高安全性。基于溶瘤病毒具有多重机制的优势,以及与免疫疗法联合的重大机遇,越来越多的溶瘤病毒产品走向临床阶段。
本文基于溶瘤病毒类药物的研发进展和临床现状,结合已获批上市溶瘤病毒药物和临床阶段已公布的研究数据,对溶瘤病毒类药物的临床生物分析内容和策略展开分享。
1.溶瘤病毒类药物临床生物分析内容
根据《溶瘤病毒类药物临床试验设计指导原则(试行)》,溶瘤病毒类药物在临床研究中需要进行药代动力学研究, 包括生物分布、病毒排出及感染性分析和表达产物定量;免疫原性研究,需监测溶瘤病毒载体及表达产物的免疫反应;此外,还应该对疗效相关的生物标志物,相关免疫细胞和细胞因子变化进行研究。

图1. 溶瘤病毒类药物临床生物分析主要内容
1.1生物分布和脱落
生物分布反映了药物进入人体后向各组织器官转运、代谢及蓄积的情况,病毒脱落为溶瘤病毒通过患者的分泌物 (尿液、唾液、汗液、鼻咽液等) /排泄物 (粪便等) 进行的散播。病毒脱落不同于生物分布,更侧重于病毒向第三方或对可能的环境风险的评估,考察病毒的脱落有助于指导临床研究中长期不良反应的监测。溶瘤病毒分布和脱落通常采用qPCR方法测定溶瘤病毒DNA的拷贝数,检测样本包括血液、尿液、肿瘤组织、唾液、注射表面拭子、封闭敷料拭子、口腔黏膜拭子、肛门拭子等。
溶瘤病毒在使用过程中的潜在担忧是病毒在人与人之间的传播,医护人员、密切接触者等。因此,需要对qPCR检测阳性的样本进行感染能力的检测,采用在经验证的50%组织培养感染剂量(TCID50)的检测感染性病毒,该方法可量化在50%接种的组织培养细胞中产生细胞病变效应所需的病毒量。
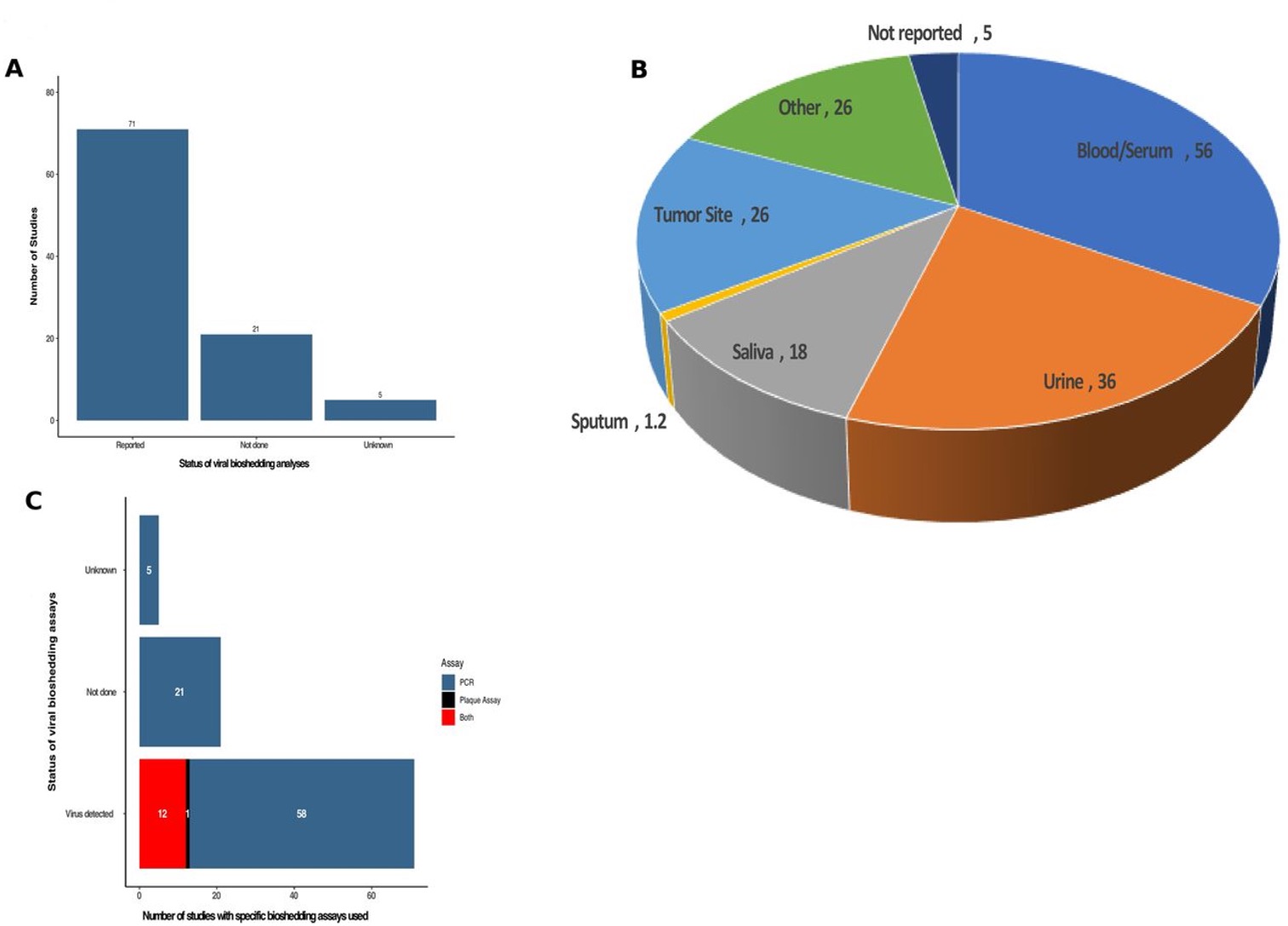
图2.溶瘤病毒临床试验中病毒脱落检测(开展脱落研究数目、脱落检测样本类型及检测方法)
如图2所示,Nicholas Macedo等人对已报告的97项溶瘤病毒临床研究进行分析,其中71项试验(73.2%)进行了溶瘤病毒的脱落研究,最常见检测部位和样本为血液,其次是尿液和肿瘤组织样本,另外有唾液、口腔拭子、痰液,脑脊液、注射部位等。在所有评估溶瘤病毒脱落的71项研究中,最常见是使用PCR方法检测特定的病毒基因组序列(58项,81.7%),斑块检测则作为PCR检测的补充用于脱落检测阳性样本的感染性分析(12项,16.9%)。
研究项目 | 具体实验内容 |
Samples | • Blood, Urine, Swabs from the exterior of occlusive dressings, surface of injected lesions, oral mucosa, anogenital area, and lesions of suspected herpetic origin. |
Biodistribution and Shedding | • Samples were tested for T-VEC DNA using a validated T-VEC–specific quantitative polymerase chain reaction (qPCR)–based assay (no detection of non-target nucleic acids, including wild-type HSV-1 and HSV-2). • The lower limit of quantification (LLOQ) of the assay (copies of T-VEC DNA/μg total DNA) is 1.76 for blood, 24 for urine, and 18 for swabs. |
Infectivity | • qPCR-positive swab samples were tested for infectious virus in the validated 50% tissue culture infective dose (TCID50) assay, which quantifies the amount of virus required to create a cytopathic effect in 50% of inoculated tissue culture cells. • Virus titer was calculated as TCID50/mL; the LLOQ for the TCID50 assay is 5,940 TCID50/mL in swab samples. |
HSV seropositive | • At baseline, 40 patients (67%) were seropositive for HSV-1, and 20 (33%) were seropositive for HSV-2. |
表1:T-VEC在黑色素瘤患者临床试验中的生物分布、脱落和传播性检(EBioMedicine 47 (2019) 89–97)
1.2表达产物检测
溶瘤病毒携带的功能基因片段,在体内通过表达产物发挥药效作用。为了增强机体的免疫应答能力,溶瘤病毒可以携带某些增强机体免疫能力的基因及其表达产物,如细胞因子IL-12、IFN-γ、GM-CSF,趋化因子CCL5和HSP等;为阻止肿瘤细胞的免疫逃逸,可携带免疫抑制基因及表达产物,如抗PD-1/L1、抗CTLA-4基因等,最终达到调节免疫能力和清除肿瘤细胞的目的。
溶瘤病毒基因表达产物检测能够为临床剂量选择提供最直接的证据支持。基因表达产物水平过低将无法达到药效剂量水平,过高将可能带来额外的安全风险。基因表达产物水平的长期监测将为临床有效性和安全性提供支持。基因表达产物水平的监测不仅仅限于浓度水平,更需要在功能水平进行监测,是否对携带基因进行修饰,基因表达产物和天然产物是否存在差异,功能活性是否相似,表达产物检测时是否需要排除内源性干扰。此外,溶瘤病毒基因表达产物水平较低,往往需要较高灵敏度的检测方法。
1.3免疫原性分析
针对溶瘤病毒的免疫反应是溶瘤病毒类药物临床试验中重要的检测项。如图3所示,Nicholas Macedo等人总结了溶瘤病毒临床试验中报告体液免疫和溶瘤病毒细胞特异性免疫应答的研究数量。在评估的97项研究中,63项(64.9%)的进行了抗病毒抗体滴度的测量,其中27项(27.8%)评估了中和抗体,其余研究评估结合抗体滴度。溶瘤病毒特异性T细胞反应的评估不太常见,仅在10项(10.3%)临床试验中报告。
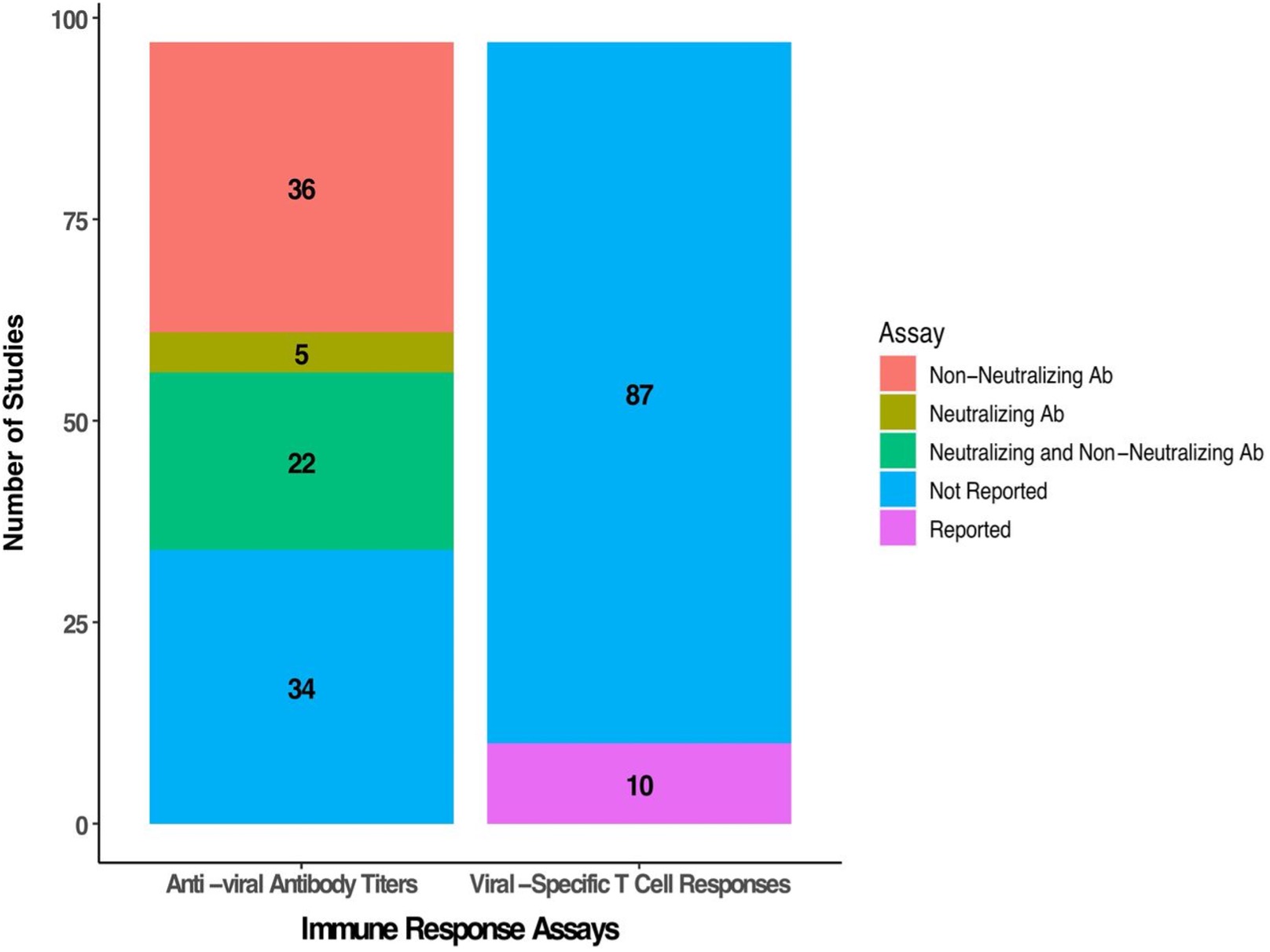
图3.溶瘤病毒临床试验中病毒体液免疫和细胞免疫检测
溶瘤病毒通常为局部注射,通过直接裂解肿瘤和激发人体的免疫系统协同发挥药理学作用,机体产生对于溶瘤病毒的病毒载体的体液免疫可以限制病毒载体在人体中的扩散,某种意义来说是安全性指标,通常体液免疫原性检测只用于病人用药后的监测。
此外,静脉注射为更大范围的肿瘤组织靶向、更广泛的溶瘤病毒药物传播、以及更便捷的注射方式提供了更有效的途径,成为仅次于瘤内注射的给药方式。然而,机体对溶瘤病毒载体预存的体液免疫会影响发生中和抗体反应,阻止药物进入细胞内,降低转染效率进而降低药效,进行影响到药物的有效性。在给予治疗后,机体经过适应性免疫应答也会产生特异性结合抗体,影响给药次数和给药间隔。
体液免疫反应主要有两种类型,结合抗体或中和抗体。中和抗体与溶瘤病毒结合并通过多种机制抑制病毒载体转导靶细胞。非中和抗体与溶瘤病毒结合并在不阻断溶瘤病毒转导的情况下“标记”病毒。对于体液免疫原性,检测的内容包括抗病毒载体结合抗体/总抗体、抗病毒载体中和抗体和抗表达产物抗体。LBA法可用于检测抗病毒载体总抗体,细胞法用于检测抗病毒载体中和抗体。
如图4所示,对于结合抗体,一般可用商业化的病毒衣壳蛋白或溶瘤病毒药物作为捕获试剂,结合待测样品中的抗病毒载体抗体,再利用通用二抗进行显色反应,用滴度值评价抗病毒载体抗体的水平,通过比较溶瘤病毒给药前后抗体滴度水平的变化来评价抗病毒载体抗体的产生情况及相对浓度水平。
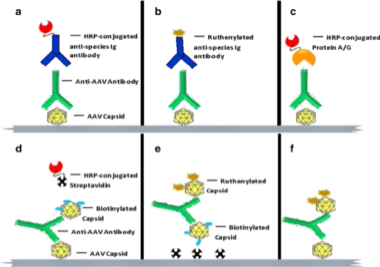
图4. 结合抗体/总抗体检测方法
相对于结合抗体检测,中和抗体更加具备生理学意义的同时,在临床生物分析过程中方法学开发,验证和数据解读也会变得更加复杂。在临床生物分析实践过程中,通常会采用表达CMV-Luc的假病毒用来模拟基因治疗药物的病毒载体或者真实病毒,假病毒和被模拟替代的病毒有类似的衣壳蛋白或者关键侵染细胞的蛋白。假病毒和待测血清样品孵育,加入靶细胞中,如果假病毒能够感染细胞,将会表达luciferase,加入检测试剂后会出现信号值,血清未起到阻断假病毒感染细胞的生理学作用。如果加入检测试剂后会出现信号值,血清中存在中和抗体,阻断了假病毒能够感染细胞,人血清中中和抗体的强度和信号值呈负相关,通过血清样品检测信号值的转化计算,可以获得血清样品中抗基因治疗药物病毒载体的中和抗体滴度值。检测原理和检测体系如图5所示:
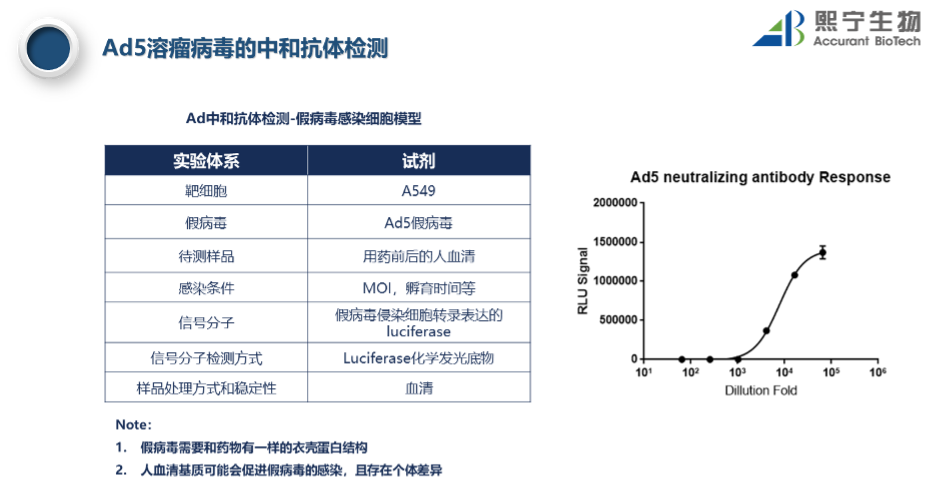
小课|流式细胞术在临床PD检测的应用——组蛋白乙酰化水平的方案设计考量图5. Ad5溶瘤病毒的中和抗体检测
对于细胞免疫原性(图6),检测的内容包括针对溶瘤病毒载体T细胞应答和针对表达产物抗体T细胞应答,一般通过酶联免疫斑点检测(ELISpot)。ELISpot是通过将溶瘤病毒载体抗原或表达产物抗原与PBMCs共同孵育后,对抗原刺激的干扰素γ(IFN-γ)分泌细胞进行检测和定量,1个斑点代表1个活性细胞,从而计算出针对特异性抗原分泌IFN-γ起反应的细胞数。

图6. ELISPOT检测细胞免疫原型
1.4药效学分析
溶瘤病毒类药物通常具有双重作用机制,以T-VEC为例,首先直接感染和杀死肿瘤细胞(溶瘤作用),其次通过诱导局部和全身免疫反应(免疫治疗效应)。T-VEC 通过局部注射到黑色素瘤的皮肤、皮下或淋巴结部位给药,在肿瘤细胞内复制T-VEC,HSV溶瘤病毒的复制导致被感染的肿瘤细胞裂解,然后释放可溶性肿瘤相关抗原、危险信号和坏死肿瘤细胞片段,所有这些都有助于启动局部免疫反应。GM-CSF的局部表达进一步增强了树突状细胞的迁移和成熟,然后树突状细胞行进到淋巴结区域,将抗原呈递给特定的 CD4+T 辅助细胞和 CD8+T 效应细胞,触发全身性 T 细胞反应。
对于此过程中相关的细胞因子、特异性T细胞反应,可使用Luminex,MSD,EnVision,Simoa,流式细胞术等方法进行检测。

2.小结
溶瘤病毒类药物的临床生物分析对于溶瘤病毒类药物的有效性和安全性至关重要。随着 T-VEC 的上市以及在更多的临床试验中取得的积极结果,溶瘤病毒作为一种新兴的肿瘤治疗手段在肿瘤免疫治疗领域表现出较好的应用前景。近年来,越来越多的研究者开始探索将一些新的病毒载体用于肿瘤治疗,并不断尝试新的基因修饰以平衡抗肿瘤免疫应答和免疫原性,以及探索不同的给药途径、新的病毒递送方式、与化疗药或免疫检查点抑制剂的联合用药等。相信随着溶瘤病毒研究的不断深入,以及溶瘤病毒临床生物分析领域研究经验的不断积累,溶瘤病毒疗法在治疗人类疾病中将会发挥更广泛、更深入的作用。
熙宁生物基于对溶瘤病毒类药物特征的充分了解,具有丰富的临床样品分析实践经验,配备全面的临床生物分析技术平台,可提供临床前、IIT和临床阶段溶瘤病毒类药物全流程、一体化的生物样品分析服务,欢迎大家后台留言咨询交流。
3.熙宁生物
熙宁生物是一家以分析科学为核心能力,专注于为生物新药临床与临床前研究提供专业技术服务的创新型CRO企业。公司主营业务包括符合国际GLP&GCP质量管理规范的生物分析(Bioanalysis,BA)服务,伴随诊断(Companion Diagnostics,CDx) 产品开发服务,以及临床前药理药效研究(Pre-clinical Pharmacology)服务。
基因治疗领域作为新兴的疗法,近些年得到了快速的发展,熙宁生物也积累了丰富的经验,和专业的技能服务能力,能够满足申办方的生物分析需求。熙宁生物搭建了满足基因治疗药物的临床检测需求和药物联用的基因检测平台,细胞/病毒检测平台,流式检测平台和免疫检测平台;通过qPCR/ddPCR技术,细胞中和抗体检测技术,ELISPOT细胞免疫原性检测技术,流式检测技术,ELISA/MSD检测技术等齐备的技术互联;能够实现通过一支技术团队,在一个生物分析实验室,为一个临床项目,提供基因治疗产品临床生物分析的完整解决方案。
4.参考文献
•Clinical landscape of oncolytic virus research in 2020
•Biodistribution, shedding, and transmissibility of the oncolytic virus talimogene laherparepvec in patients with melanoma
•Pharmacokinetic drug evaluation of talimogene laherparepvec for the treatment of advanced melanoma
•Oncolytic viruses challenges and considerations in an evolving clinical landscape
•ICH Considerations Oncolytic Viruses international conference harmonization technical requirements registration pharmaceuticals human use
•《溶瘤病毒类药物临床试验设计指导原则(试行)》
•《溶瘤病毒产品药学研究与评价技术指导原则(试行)》