



多重免疫组化(multiplex immunohistochemistry, mIHC)是近年来兴起的一种多重荧光标记的免疫组化染色方法,是肿瘤药物临床开发过程和临床前研究的重要工具,已被众多药企广泛应用于肿瘤免疫微环境研究、新靶点探索,以及更多新的免疫治疗方案的挖掘。
PART 01
mIHC技术简介及基本原理
多色免疫荧光有多种技术路线,目前最为成熟的方法是基于酪胺信号放大技术(tyramide signal amplificatio, TSA)。该技术利用二抗上标记的辣根过氧化物酶(HRP)催化底物过氧化氢,使加入反应体系的带有荧光标记的酪胺被氧化为活化状态,并能与组织样本中富含的酪氨酸残基共价结合,从而在特定的抗原位置形成荧光信号。该信号不受微波影响,因此可通过微波加热去除抗体再进行下一轮的一抗、二抗孵育(图1, 2)[1]。
基于TSA技术可在组织切片上孵育多种不同标记物抗体,再结合高分辨率多通道的荧光扫描技术和分析软件,可以对多种生物标记物在肿瘤微环境中的表达状态进行检测分析,从而揭示肿瘤的发生发展,肿瘤免疫微环境,或者药物的药效等多种生理病理过程。
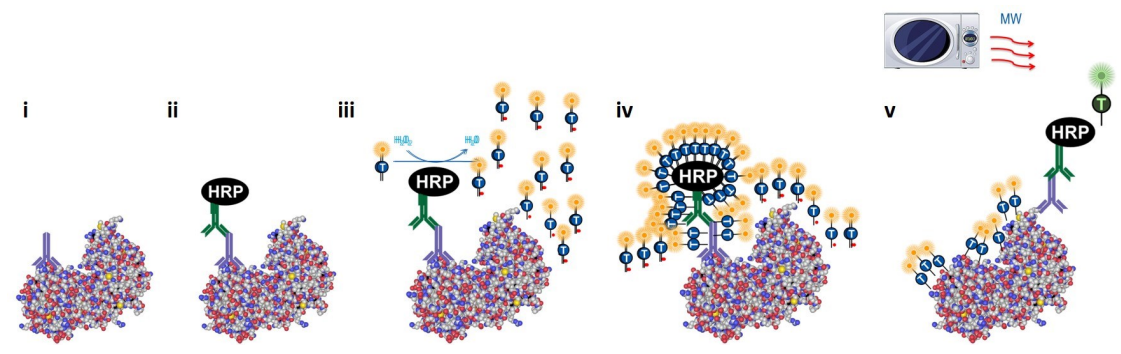
图1 mIHC技术原理示意图
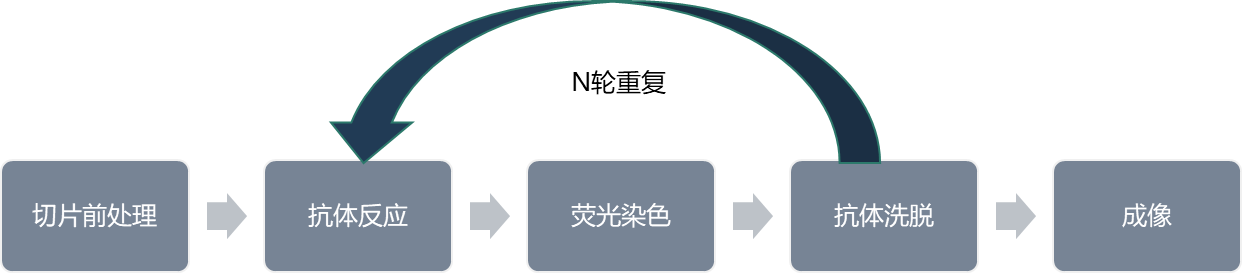
图2 mIHC实验流程
PART 02
mIHC技术的优点和局限性
传统免疫组织化学 (IHC) 是组织病理学中广泛使用的诊断技术。然而,该技术存在许多局限,比如观察者间的高变异性,以及每个组织切片仅标记一个指标。相比较传统的单染免疫组化,mIHC可以提供大量多靶标的空间位置、定量分析、细胞类型分布等大量信息,因此在临床研究上受到越来越多的重视。

mIHC技术可以提供更大信息量,更高精准度,
同时需要更少组织量
传统IHC技术想要获得多个靶点信息需要在多张切片上进行染色,并将染色结果对比着观察,易受切片不连续的影响造成偏差。而mIHC可在一张切片上同时获得关于细胞定量、细胞亚群分型、细胞空间排列等多个类型的信息,结果更准确,同时也能极大的节省样本需求量。与明场多重染色相比,前者需要使用不同种属的一抗来避免二抗的交叉反应,而mIHC由于每一轮染料标记上后都会通过微波加热去除结合的抗体再进行下一轮标记,故使用的抗体不受种属限制,选择起来更加便利。此外,mIHC染色结果配合智能图像分析软件使用,定量评估细胞密度、表型和定位等,相比传统病理医生的人工判读更加精准。

mIHC技术有更好的预测价值
一项基于文献研究(总计超8000例患者)的Mata分析显示,当采用传统免疫组化、肿瘤突变负荷(tumor mutational burden, TMB)、基因表达谱(gene expression profiling, GEP)或肿瘤微环境来预测免疫检查点抑制剂的疗效时,基于mIHC的肿瘤免疫微环境分析具有最高的预测价值,甚至比前三者联合的预测效果还要好(图3),充分展示了mIHC技术可视化、定量、高通量的优势[3]。
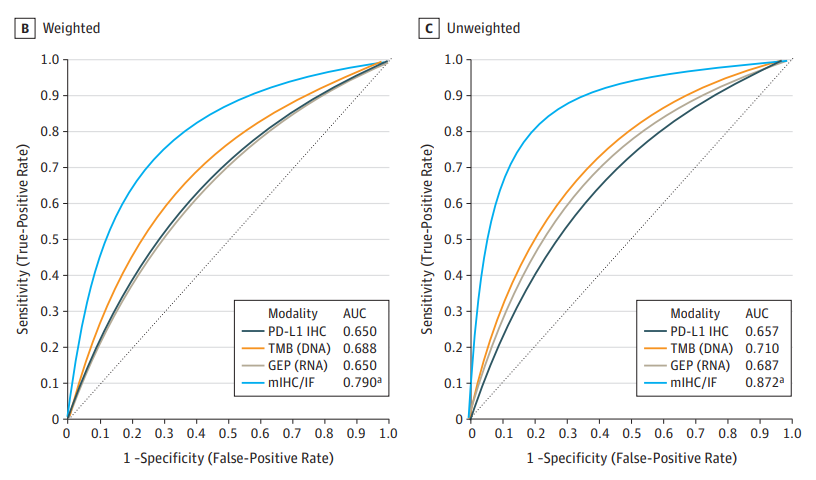
图3 mIHC预测效果最佳

mIHC技术操作复杂,投入高
mIHC技术发展至今也存在一定的局限性,譬如由于需要反复多轮的抗体孵育和荧光染料标记使得整个实验流程耗时较长,且当标记的荧光种类较多时不可避免地会出现波长相近荧光信号的串扰。同时,mIHC染色结果需要通过扫描仪捕获并利用智能软件分析处理,要得到的巨大信息量的数据对实验室配套硬件设施的存储能力及计算能力要求均较高,实验成本也较高。因此如果需要获得高质量的mIHC结果,要在全自动化的染色仪器进行染色,尽量减少手工操作带来的不确定性。同时,必须配备智能化的分析软件,并对分析过程严格控制,从而实现对图像数据的标准化分析。
PART 03
mIHC技术的应用
目前,mIHC技术已经在多个领域发挥了重要作用,如肿瘤免疫微环境的变化、受试者用药前后的相关靶标的表达差异、免疫细胞的浸润情况、三级淋巴结结构研究、信号通路中关联靶点的空间分析等。下文将展示几个例子以供大家参考。

用药前后肿瘤免疫微环境变化
肿瘤微环境(tumor microenvironment, TME)包括肿瘤相关巨噬细胞、成纤维细胞、肿瘤浸润淋巴细胞、髓源性抑制细胞、肥大细胞等,是多种类型细胞相互作用形成的动态网络,尤为适合采用善于分析复杂样本的mIHC技术进行研究。例如通过定量分析HER2阳性乳腺癌患者肿瘤组织间质和瘤内浸润的免疫细胞(包括CD8+的细胞毒T细胞、CD4+/FoxP3-的辅助T细胞、FoxP3+的调节性T细胞、CD20+的B细胞及CD68阳性的巨噬细胞)的密度,可揭示不同细胞亚群对免疫治疗的响应程度、探寻疗效预测的标记物。当与基因组分析方法联合对经抗PD-1药物治疗的黑色素瘤患者进行研究时,发现PTEN突变往往伴随着不良预后,这也与免疫抑制的肿瘤微环境相关[2]。
此外,将mIHC技术运用于靶向治疗的各个阶段观察免疫细胞,可为治疗提供更精准的路线图。如在转移的肺癌患者中通过panel: DAPI/CK/CD14/CD8/CD3的染色发现药物治疗响应阶段可见活化的T细胞和减少的巨噬细胞,而耐药阶段则出现相反的现象[2]。
在一项针对可手术的非小细胞肺癌新辅助治疗(纳武利尤单抗单独或联用伊匹木单抗)II期临床试验研究中,采用mIHC技术检测了治疗前后的肿瘤组织样本,发现在两种药物联合治疗后,CD3+及CD3+CD8+的TILs显著增加,且出现CD3+CD8+CD45RO+记忆TILs密度增高的趋势。与此同时,联合用药也可诱导不同免疫细胞亚群的浸润,如CD3+CD8+PD-1+的T细胞、CD3+CD8+GZB+的T细胞、CD3+CD8-FoxP3+的T细胞、CD68+及CD68+PD-L1+的细胞。而单独使用纳武利尤单抗治疗前后,免疫细胞亚群没有实质性的改变。可见mIHC技术可用于观测治疗后的免疫响应程度,从而对预后做出评估,有助于个体化用药/治疗的实施[4]。
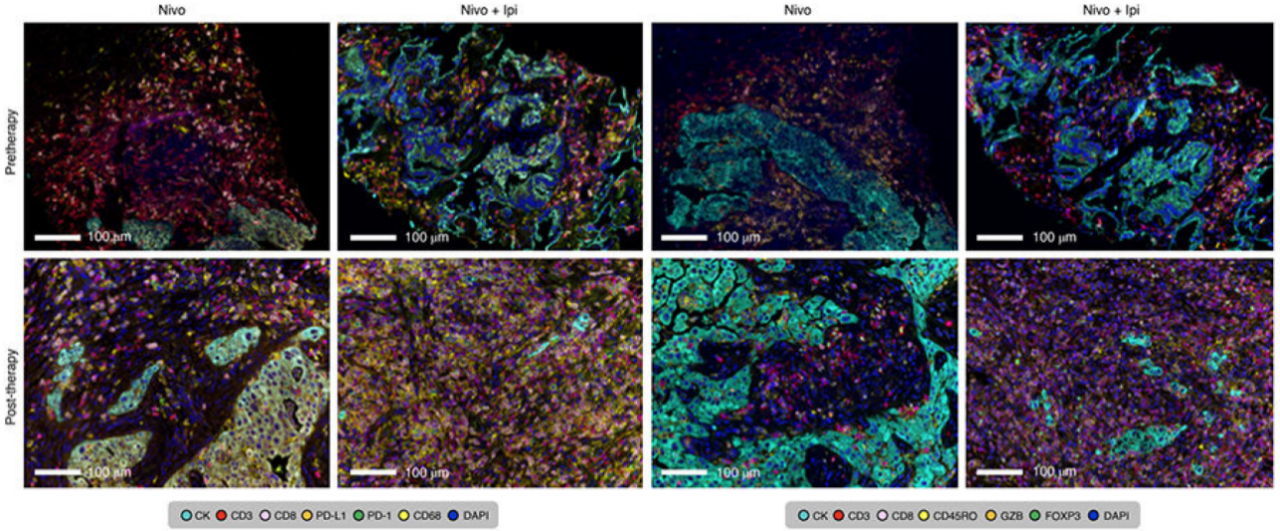
图4 利用mIHC观测治疗前后多个靶点蛋白的表达水平变化

肿瘤相关免疫细胞空间位置与预后价值
利用空间分布研究恶性细胞和肿瘤相关免疫细胞(TAIC)之间的相互作用对于确定肿瘤进展、复发或生存的可能性至关重要。免疫细胞的分布模式影响癌症患者的预后在多种肿瘤中被证实,如乳腺癌,肺癌,结直肠癌。
在一项研究[5]中,使用包含在5个mIHC panel(图5)中的 23 种标记物(包括 T 细胞、B 细胞、免疫检查点和骨髓细胞标记物)分析了一组肿瘤组织芯片(TMA),其中包含从大量 I-III 期 NSCLC 患者中获取的肿瘤样本。根据23种标记物针对相关的肿瘤细胞和免疫细胞进行分析,通过将细胞分布模式与细胞距离相结合,确定了四组细胞免疫模式:
· 第 1 组:与恶性细胞中位距离较近的混合模式;
· 第 2 组:与恶性细胞中位距离较远的混合模式;
· 第 3 组:与恶性细胞的中位距离接近的非混合模式;
· 第 4 组:与恶性细胞的中位距离较远的非混合模式。
进一步的研究发现,第 2 组与其他组相比占比较高,在 36.8% 的患者中观察到这一组,其特征是 T 细胞表型密度高,但恶性细胞表达的免疫检查点密度低,这表明第 2 组模式可能显示了该类型肿瘤的炎症效应。第 1 组(与恶性细胞中位距离接近的混合模式),在 23.6% 的样本中观察到;第 3 组(与恶性细胞中值距离接近的非混合模式),在 9.0% 的样本中观察到。相比之下,第 4 组总体显示 T 细胞密度最低,但恶性细胞表达的免疫检查点密度最高,表明第 4 组模式显示“冷”肿瘤的特征。生存曲线结果显示,在 ADC 中,CD3 + CD8 + 细胞毒性 T 细胞、CD3 + CD8 + GZB + 激活的细胞毒性 T 细胞和巨噬细胞与恶性细胞的近距离与远距离相比,与更好的 OS 相关,这表明这些细胞与细胞的接近,减轻了抑制细胞的抑制作用。恶性细胞与 B7-H3 + T 细胞的距离较近与 OS 较差相关(图5)。该研究表明空间表型研究可以很好的研究肿瘤微环境及患者预后的情况,为新诊疗策略的提出奠定了基础。
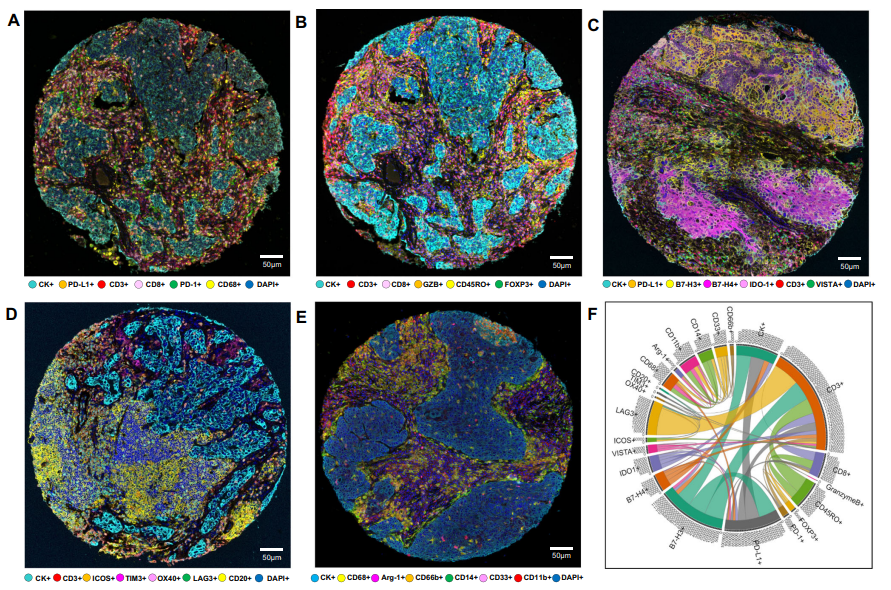
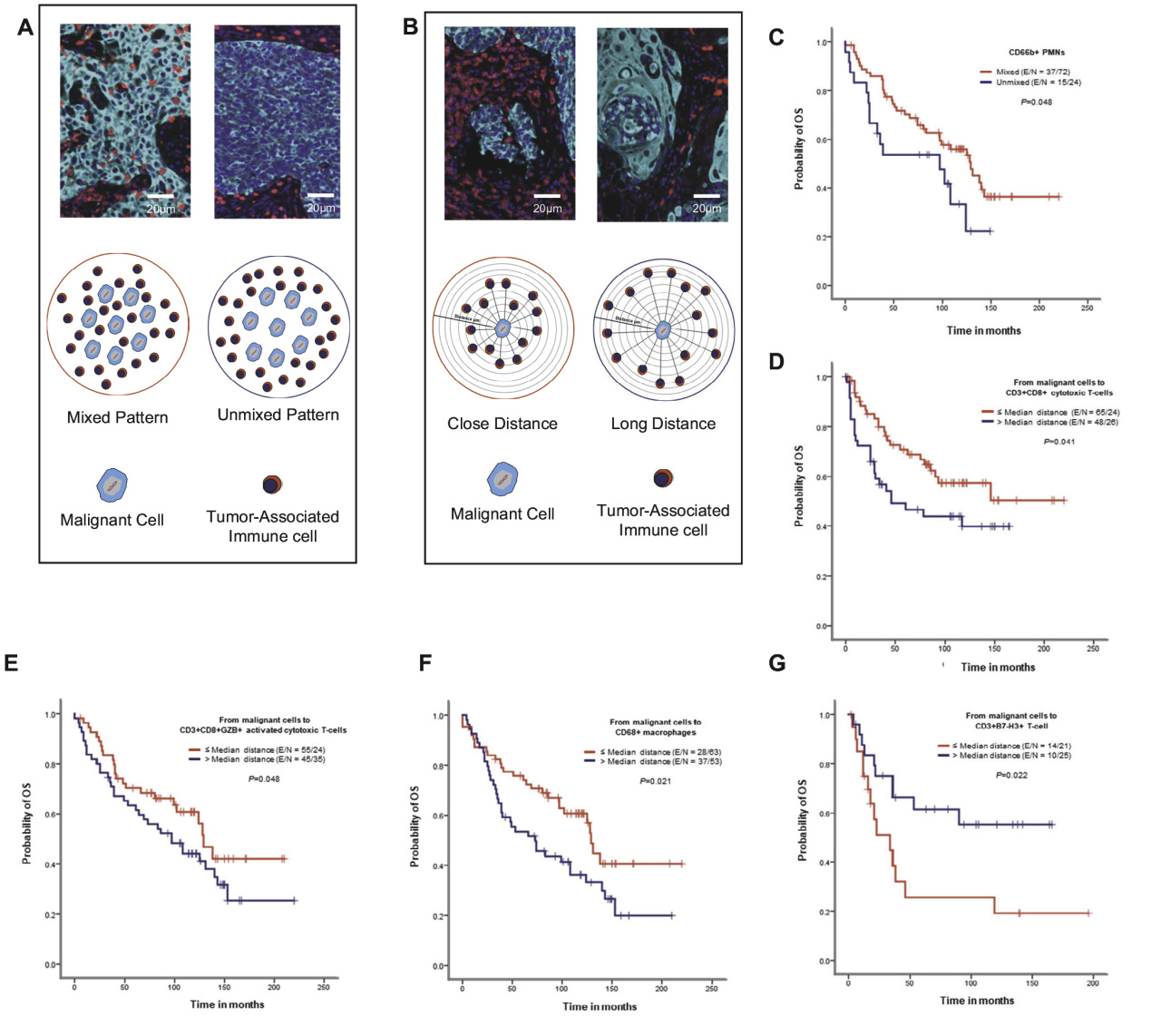
图5 利用mIHC panel分组分析肿瘤患者免疫细胞空间位置与预后相关性

三级淋巴结构与预后
三级淋巴结构(tertiary lymphoid structures, TLSs)是免疫肿瘤学领域的一个热门话题,它在影响肿瘤微环境中起着至关重要的作用。TLS已在多种实体瘤类型中被发现,当存在于肿瘤微环境中时与更好的生存相关。mIHC技术可用于评估肿瘤组织的三级淋巴结构,并在三级淋巴结构的研究中发挥了重要作用[6]。
一项研究[7]分析了从 328 名接受抗 PD-1 或抗 PD-L1 抗体治疗的患者获得的治疗前存档肿瘤样本,研究发现105 例患者 (32%) 中存在 TLS,其中 84 例具有成熟 TLS (25.6%)。在成熟 TLS 组中, 84 名患者中有 31 名 (36.9%; 95% CI, 26.6%–48.1%) 获得客观缓解,而 21 名TLS 不成熟患者中有 4 名获得客观缓解 (19.3%; 95% CI, 5.4%–41.9%),223 名TLS 阴性患者中有 43 名获得客观缓解(19%;95% CI,14.3%–25.1%),三组中的比例有显著差异(p=0.015),据此可见TLS的存在与免疫治疗的预后有明显相关性(图6)。
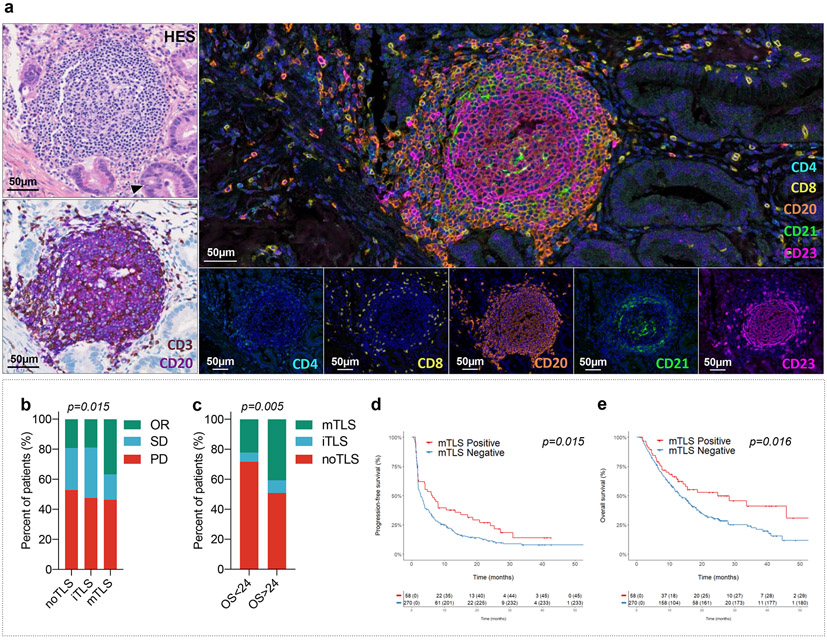
图6 成熟的 TLS 可评估癌症患者免疫治疗预后
总之,多重免疫组化可实现在一张FFPE切片上同时、原位地检测多个指标。该方法通过结合多种标志物在细胞上的表达状况识别不同细胞亚群,同时结合智能分析软件,统计各个组织区域中细胞类型、 密度、空间位置关系等信息,获得大量原来单标染色不具备的细胞类型,密度,空间距离等信息,从而使研究者对于目标区域的认识上升到一个新的维度,在药物临床和临床前的研究方面得到了广泛应用。
PART 04
熙宁生物|精翰生物mIHC平台简介
熙宁生物|精翰生物组织病理实验室mIHC平台配备了高标准的徕卡Bond Rx全自动免疫组化染色机、Akoya PhenoImager全光谱成像系统以及Halo数字病理图像分析平台等重量级设备及分析系统,可提供自动化,高质量的mIHC研究全流程解决方案。从panel设计,panel验证,以及样本检测等提供全方位的支持。可为广大药企提供高品质的临床前、临床试验阶段的组织样本mIHC检测,欢迎垂询。
图7 熙宁生物|精翰生物mIHC平台主要仪器设备
参考文献:
[1] 孙文佳,周建娅,周建英.多色标记免疫组织化学染色和免疫荧光染色在肺癌免疫治疗中的研究进展[J].中国肺癌杂志, 2021, 24(1):7.
[2] Li W, Yuan X, Xu B, et al. Applications of multiplexed immunohistochemistry/immunofluorescence and multispectral imaging technology in the field of tumor immunotherapy[J]. Journal of Chinese Pharmaceutical Sciences, 2020, 29(10).
[3] Lu S, et al. Comparison of Biomarker Modalities for Predicting Response to PD-1/PD-L1 Checkpoint Blockade: A Systematic Review and Meta-analysis. JAMA Oncol. 2019 Aug 1;5(8):1195-1204.
[4] Cascone T, et al. Neoadjuvant nivolumab or nivolumab plus ipilimumab in operable non-small cell lung cancer: the phase 2 randomized NEOSTAR trial. Nat Med. 2021 Mar;27(3):504-514.
[5] Parra ER, Zhang J, Jiang M, Tamegnon A, Pandurengan RK, Behrens C, Solis L, Haymaker C, Heymach JV, Moran C, Lee JJ, Gibbons D, Wistuba II. Immune cellular patterns of distribution affect outcomes of patients with non-small cell lung cancer. Nat Commun. 2023 Apr 25;14(1):2364.
[6] Sautès-Fridman C, Petitprez F, Calderaro J, Fridman WH. Tertiary lymphoid structures in the era of cancer immunotherapy. Nat Rev Cancer. 2019 Jun;19(6):307-325.
[7] Vanhersecke L, Brunet M, Guégan JP, Rey C, Bougouin A, Cousin S, Moulec SL, Besse B, Loriot Y, Larroquette M, Soubeyran I, Toulmonde M, Roubaud G, Pernot S, Cabart M, Chomy F, Lefevre C, Bourcier K, Kind M, Giglioli I, Sautès-Fridman C, Velasco V, Courgeon F, Oflazoglu E, Savina A, Marabelle A, Soria JC, Bellera C, Sofeu C, Bessede A, Fridman WH, Loarer FL, Italiano A. Mature tertiary lymphoid structures predict immune checkpoint inhibitor efficacy in solid tumors independently of PD-L1 expression. Nat Cancer. 2021 Aug;2(8):794-802.