



近日默沙东与 Moderna 联合公布了个体化 mRNA 癌症疫苗 mRNA-4157 联合抗 PD-1 单抗 Keytruda 用于完全切除术后的高危黑色素瘤(III/IV 期)患者的 IIb 期 KEYNOTE-942/mRNA-4157-P201 研究的中位 5 年随访数据。研究的主要终点无复发生存期(RFS)显示出有临床意义的持续改善,与 Keytruda 单药治疗相比,联用组将复发或死亡风险降低了 49%(HR=0.510;[95% CI, 0.294-0.887];p=0.0075)。安全性特征与此前报告保持一致。在术后辅助治疗领域,肿瘤疫苗联合PD1免疫治疗方案相对于免疫治疗单药方案呈现碾压式的生存获益,预示着肿瘤疫苗即将引领创新药物的时代潮流。酶联免疫斑点技术(Enzyme Linked Immunospot Assay,简称ELISPOT)是疫苗临床药物研发细胞免疫学评估中最为敏感的检测方法,也是肿瘤疫苗领域必须检测项,其重要性不言而喻。
然而,在疫苗临床研发阶段,ELISPOT检测技术进行细胞免疫评估有较多的难点:全血分离PBMC时效要求高、前处理流程复杂、PBMC样品不稳定、分析批质控体系不健全、数据分析和解读困难、阳性结果不易呈现等。
本期文章,笔者将基于熙宁生物|精翰生物(以下简称熙宁丨精翰生物)肿瘤疫苗ELISPOT检测丰富的项目经验,解析和分享ELISPOT检测的难点和项目管理要点。
熙宁|精翰生物有超过20个肿瘤疫苗临床项目在同时进行,涉及到多种药物形式,多种载体和多个技术方向。基于丰富的项目经验,汇总了肿瘤疫苗项目临床生物分析的主要内容,如下图所示:
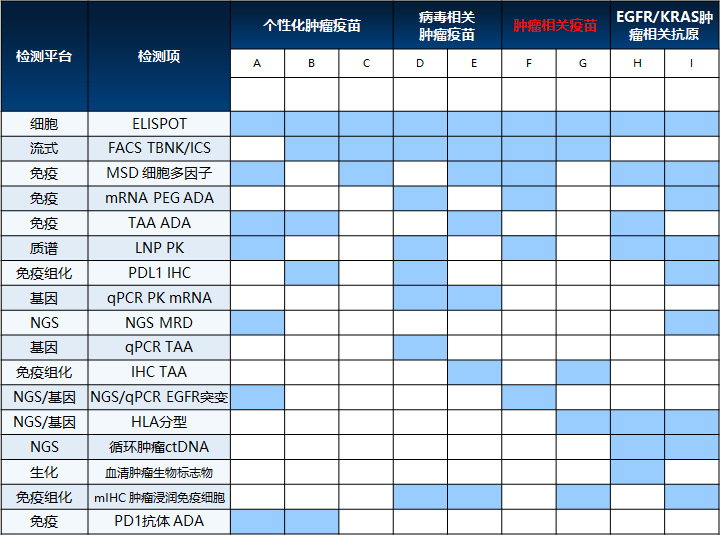
图1 熙宁|精翰生物肿瘤疫苗项目临床生物分析的主要内容
肿瘤疫苗作为复杂药物形式的代表,同时可能涉及到药物联用,需要多样化的生物分析技术进行疫苗效果和疫苗作用机理的全方位评估,生物分析内容简单总结如下:
·
ELISPOT为肿瘤疫苗评估必检项目,FACS TBNK或者更复杂的细胞分型/MSD多因子通常二选一,以满足相关法规两种免疫学评估方法的要求。
·
PEG ADA跟mRNA递送载体 相关,TAA ADA和表达产物相关,有一半的概率会测。
·
LNP PK和qPCR mRNA PK有一半的概率会测,基于药物载体的成熟程度。
·
PD1联用通常会测PD1抗体 ADA但不测PK,部分临床会进行IHC PDL1的检测。
·
肿瘤相关疫苗,特别是KRAS/EGFR突变疫苗会检测HLA分型,病毒相关肿瘤疫苗会测qPCR或者IHC测病毒阳性,作为重要的筛选入组指标。
·
作为回顾性药效指标,会涉及到循环肿瘤ctDNA,血清肿瘤生物标志物和MRD的测量,对于术后辅助治疗应用场景,可能作为关键的替代终点,需持续关注技术成熟度和法规认可度。
熙宁|精翰生物基于一体化的检测平台可提供上述所有检测项的检测服务,同时有丰富的项目管理经验,和不同检测项的结果关联解读经验。
酶联免疫斑点技术的基本原理是通过免疫细胞和对应的刺激物进行共培养,然后使用类似于ELISA双抗夹心法对有刺激反应的免疫细胞进行检测。由于免疫细胞激活机理的复杂性,根据免疫细胞的来源选择,刺激物的类型,刺激方式的不同会衍生出不同应用方向,不同灵敏度的ELISPOT检测方法,其简要的流程如图2所示:
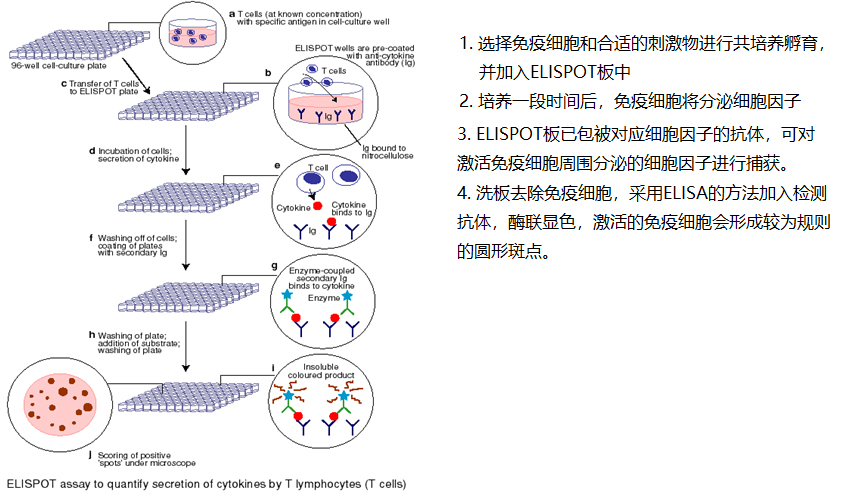
图2 ELISPOT技术基本操作流程
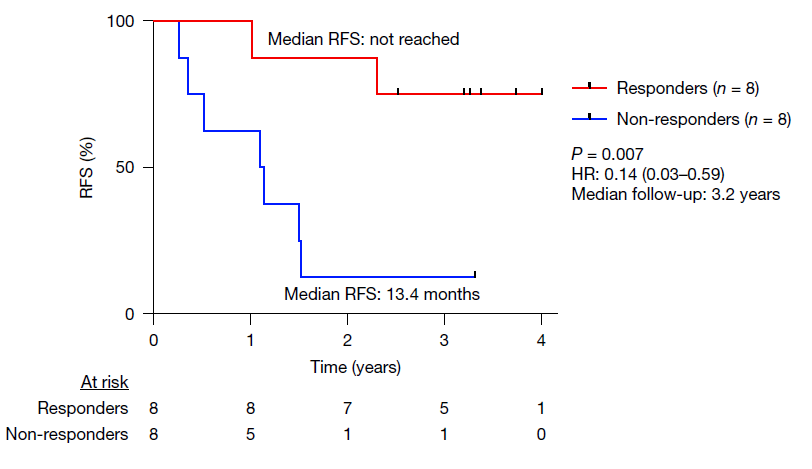
图3 基于ELISPOT的肿瘤疫苗响应者与无响应者无复发生存率对比
如图3所示,肿瘤疫苗有响应者相对于无响应者,有非常显著的临床获益,其中响应或者无响应的界定标准为ELISPOT检测项的结果是否为阳性,ELISPOT检测是肿瘤疫苗的药效动力学指标,也是患者分层分析和预后指示的有效生物标志物。
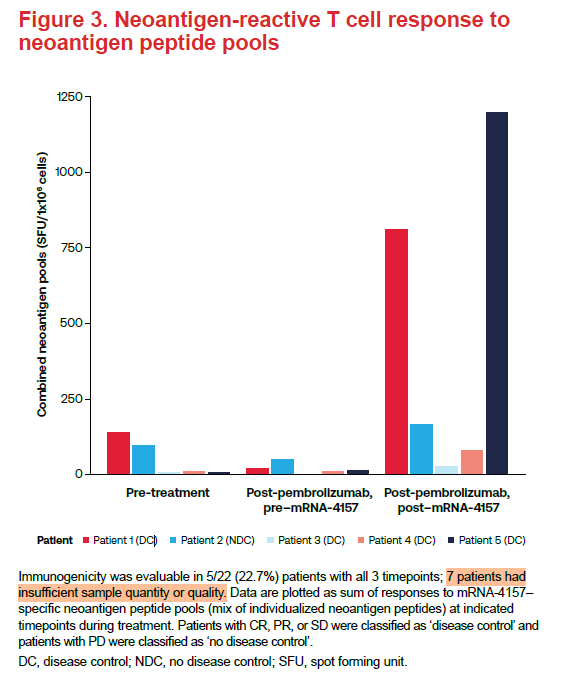
图4 T细胞对新抗原肽库的免疫应答
在肿瘤疫苗的临床生物分析中,ELISPOT检测是技术难度较高的一项,同时也容易因样品质量问题导致数据缺失。如图4所示,mRNA-4157 (V940) 披露的ELISPOT检测结果中22个受试者有7个受试者样品数量或者质量不好;剩余的受试者中5/15有ELISPOT响应;有响应的5个受试者,有4个疾病得到了控制。
从mRNA-4157 (V940)披露的ELISPOT检测结果,结合其近期披露的IIb 期临床结果,对比我司在同类型肿瘤疫苗项目上ELISPOT检测项中阳性结果响应率情况,初步判断为mRNA-4157 (V940)的ELISPOT检测结果低估了最终的临床效果,根本原因是样品质量大部分不合格,ELISPOT技术在临床样品分析领域应用和转化难度高。
熙宁|精翰生物在肿瘤疫苗评估ELISPOT项目中,做到了全流程管理。在个性化肿瘤疫苗,肿瘤相关抗原疫苗和病毒来源抗原肿瘤疫苗项目中,均获得了远高于mRNA-4157 (V940)的ELISPOT阳性率结果。同时做出了细胞免疫的药效动力学趋势,并跟给药剂量和给药周期匹配,不同受试者的整体趋势相对一致,在ELISPOT检测项临床生物分析领域为行业内最优秀的团队,部分检测结果示意图如下。
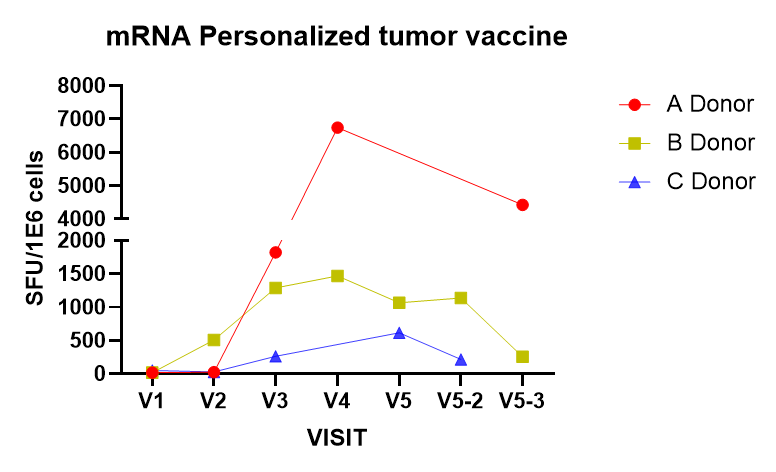
图5 个性化肿瘤疫苗,3个受试者的ELISPOT检测结果趋势
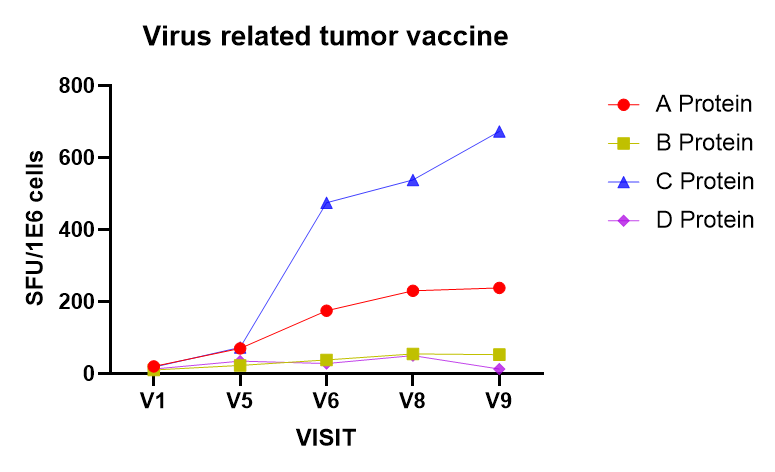
图6 病毒来源肿瘤治疗疫苗,1个受试者4个不同抗原的ELISPOT检测结果趋势
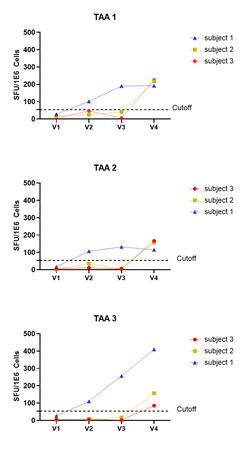
图7 TAA/TS肿瘤治疗疫苗,3个受试者3个不同抗原表位的ELISPOT检测结果趋势
·
熙宁|精翰生物每个月有400管以上的时效全血ELISPOT样品进行PBMC分离,有丰富的时效全血样品管理经验;
·
有超过40个ELISPOT检测项目在运转,有丰富的肿瘤疫苗相关的临床项目检测经验,能够对数据的整理趋势有系统性的把握和解读;
·
大部分感染性疫苗/肿瘤疫苗管线均做出来了细胞免疫药效动力学趋势,并跟给药剂量和给药周期匹配,不同受试者的整体趋势相对一致。
基于大量临床项目的管理ELISPOT技术用于临床样品分析有以下难点要点,以及对应我司的解决方案。

难点1
全血需8小时以内分离PBMC才能确保完整的功能活性,中心医院和临床CRC没有熟练的技能和设备支持全血分离PBMC。
熙宁|精翰生物解决方案:开发了全血稳定剂,可将全血放置时间延长到48小时,将全血48小时内寄送到精翰进行分离。全血放置稳定性经过了正式方法学验证,同时经历了超过5000个临床样品检验论证其可靠性。对于肿瘤适应症,临床中心较多,受试者人员分散,同时采血时间分散,持续时间长,将全血样品寄送到精翰进行集中分离和管理也是成本效率更优的选择。
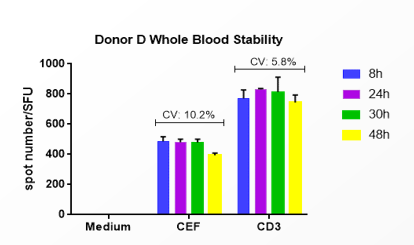
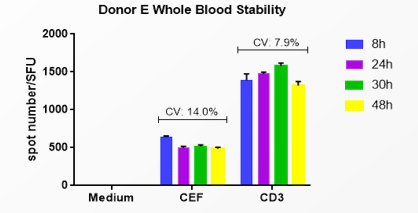
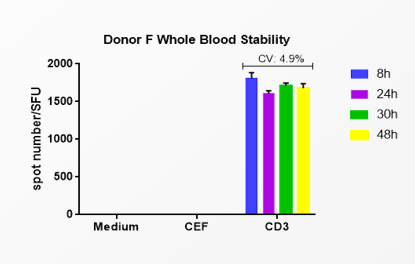
图8 熙宁|精翰生物自主ELISPOT方法学全血放置稳定性数据

难点2
全血分离PBMC不能经过冻存,需要新鲜进行检测,中心医院无技术能力和仪器支持,寄送到检测单位进行,物流,分离和检测均耗时耗力,检测人员需要通宵进行试验,项目管理模式不可持续,人员流动性大,组织结构不稳定。同时随到随检,成本高昂。
熙宁|精翰生物解决方案:开发了PBMC液氮冻存稳定性技术,PBMC可放置在液氮环境保存,有1年的稳定性,PBMC液氮冻存稳定性经过了正式方法学验证,同时在研发阶段对比过新鲜检测和冻存检测结果可比性,经历了超过5000个样品检验论证其可靠性。对于肿瘤适应症来说,可以将同一受试者不同访视点的样品集中在同一个分析批检测,结果更加可比,性价比更高。同时批量进行检测,通量高,人员作息规律试验质量有保证,组织结构持续性好,匹配临床较长的采样周期,维持检测结果长期一致。

难点3
样品分析过程中无真实质控样品,仅使用阴性对照作为质控,样品分析的质控标准非常松,无失败的可能性,检测结果不可控不可比,不同访视点的数据随机分布。
熙宁|精翰生物解决方案:精翰基于CEF刺激阳性PBMC设置了质控样品,并进行了定值作为替代质控样品,每个分析批样品分析均会带上质控样品,进行了较为严格的质控,确保不同分析批不同时间点做出的质控样品结果可比,外推到样品分析结果可比。
ELISPOT检测技术用于临床样品分析,除了满足定性(阴阳性)判定需求,还需有定量(斑点多少的比较)检测需求。这需要更加严格的方法学验证和样品分析体系对样品分析的结果进行评估,比如样品的阴阳性判定阈值LOD,样品功能活性判定标准MIR等,是一个精密复杂的体系,需要有完善的体系构建。熙宁|精翰生物基于行业白皮书建立ELISPOT的验证体系,验证体系的数据作为样品分析的核心判定参数,同时基于临床样品分析的实际情况进行了全血放置稳定性,液氮冻存稳定性相关的验证,对ELISPOT样品,从中心采集到最终检测数据汇报和分析,搭建了全流程的管理体系,并取得了优效的临床样品分析结果,能够真实客观的代表肿瘤疫苗药物在人体的细胞免疫情况,欢迎咨询。
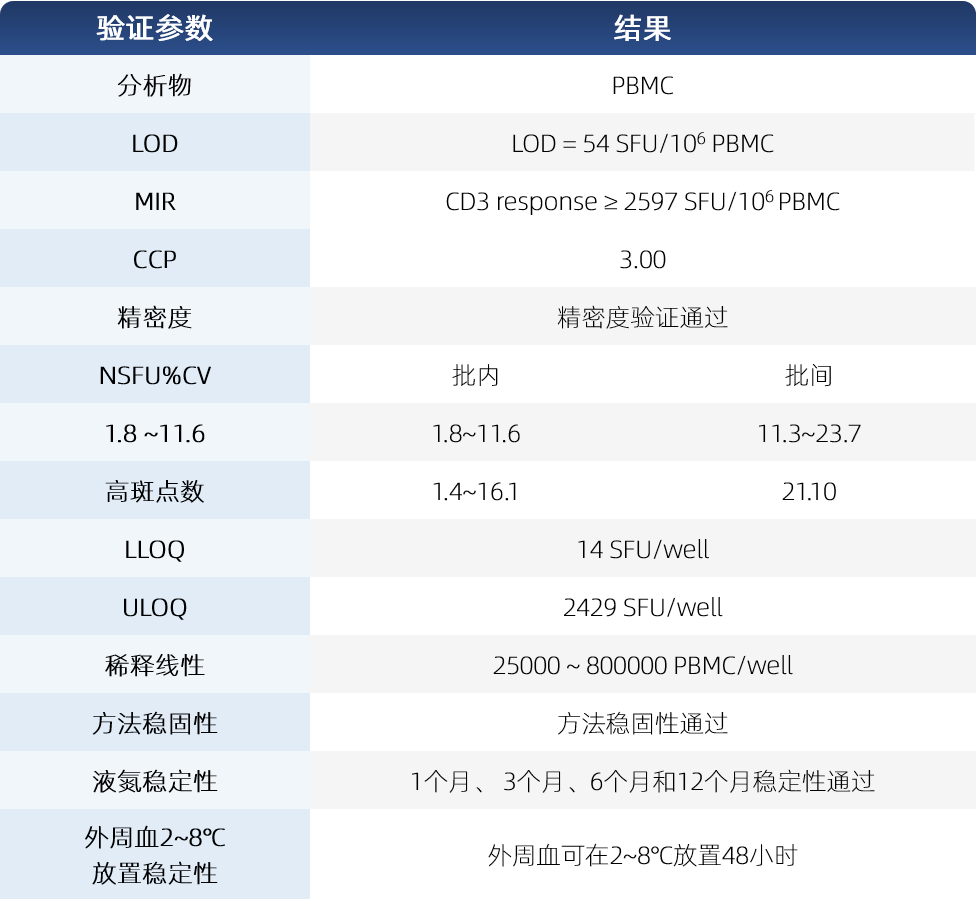
图9 熙宁|精翰生物ELISPOT自主方法学验证主要参数