



靶向蛋白质降解(TPD)目前主要通过泛素蛋白酶体和溶酶体降解目标蛋白,根据具体作用原理又可细分为近10个不同技术路线,其中发展最快的是分子胶和PROTAC技术。
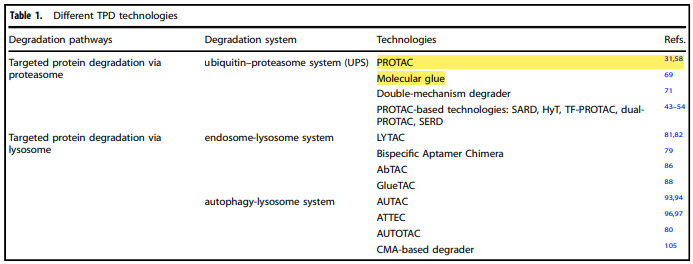
图1 靶向蛋白质降解(TPD)不同的技术路线
分子胶 VS PROTAC:
➢
分子胶不需要与POI存在亲和力。
➢
分子胶在成药性上优于PROTAC。
➢
分子胶大多数是偶然发现的,而PROTAC可以通过合理设计实现。
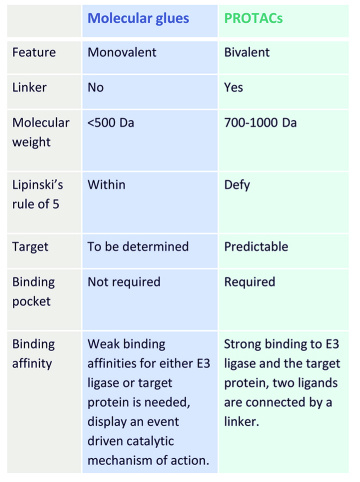
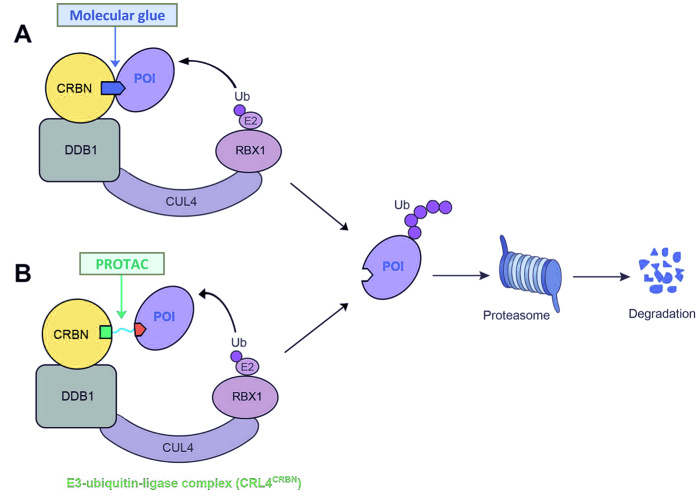
图2 分子胶 VS PROTAC
PART 01
全球范围内分子胶和PROTAC药物研发情况概览

全球分子胶药物研发情况
目前研发的新药大多通过E3的组成分子CRBN来降解蛋白质,主要用于MM、血液系统肿瘤和实体恶性肿瘤等疾病治疗。从作用机制来看,IKZF1/3是其中最热门的作用靶点,GSPT1、DCAF15、IKZF2、BCL-xL、SEL1L2等新靶点也陆续被开发。
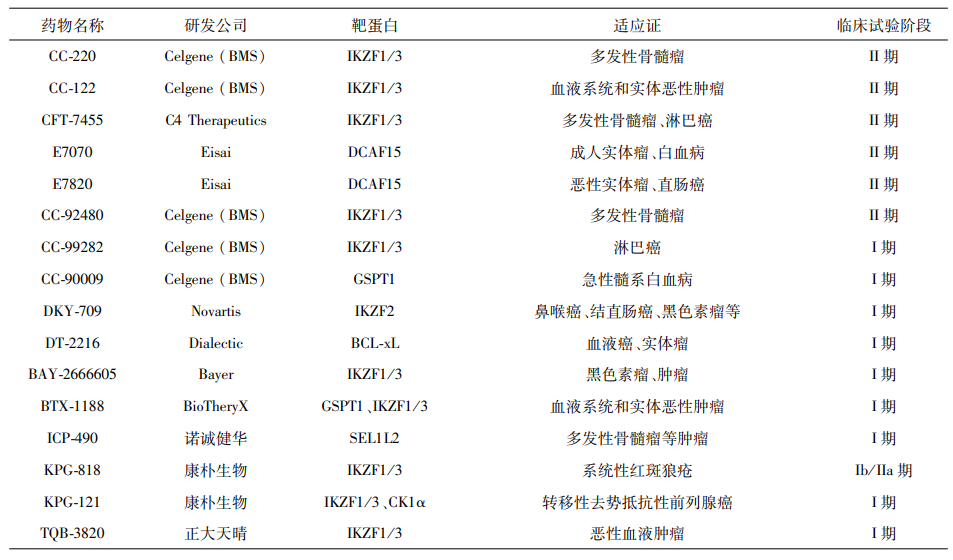
图3 全球分子胶药物研发情况(不完全统计)

全球PROTAC药物研发情况
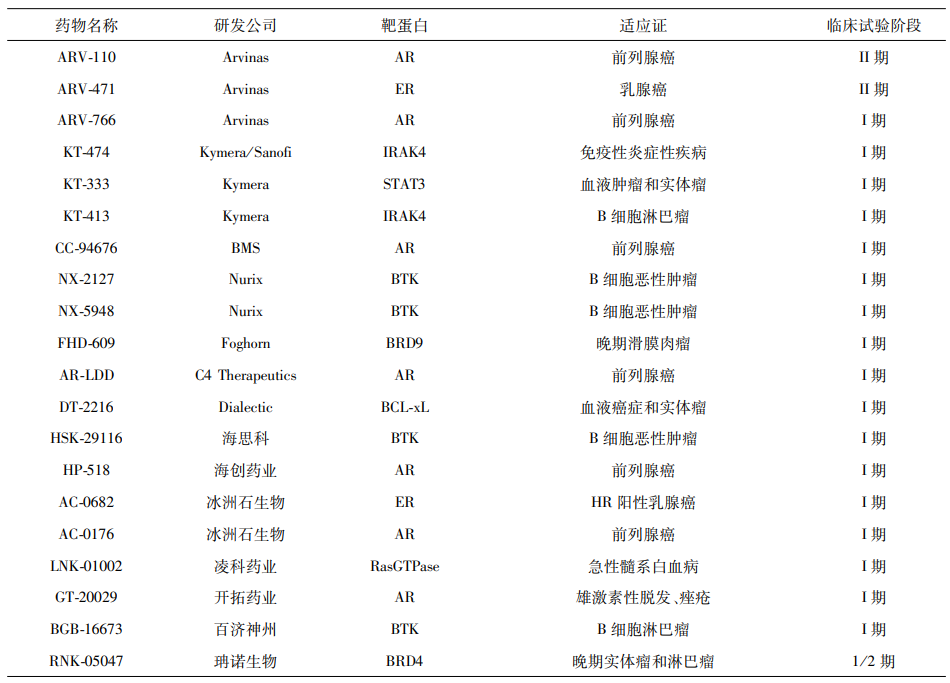
图4 全球PROTAC药物研发情况(不完全统计)
PART 02
流式细胞术在分子胶和PROTAC药物PD检测中的应用

流式细胞术在SP-3164 PD研究中的应用
SP-3164是一种阿伐度胺(AVA, CC-122)的氘稳定(S)对映异构体,同时也是一种可口服的分子胶,用于降解Ikaros和Aiolos(I/A)。相关体外研究数据表明其在多发性骨髓瘤临床前模型中具有活性,与来那度胺(LEN)、泊马度胺(POM)和阿伐度胺(AVA)相比,SP-3164更有效、更快速地降解促癌转录因子I/A,而稳定的(R)-对映异构体SP-3165既不结合CRBN也不降解I/A。在初步的体内研究中,SP-3164产生了显著的肿瘤生长抑制(TGI)。
将SP-3164降解MM.1S细胞中Aiolos的潜力与SP-3165、AVA和POM进行了比较。SP-3164以时间和剂量依赖性方式快速而有力地降解Aiolos,比AVA和POM更有效,而SP-3165表现出最弱的Aiolos降解。为了研究SP-3164对细胞存活的影响,用SP-3164(0.1μM、1μM和10μM)和SP-3165(1μM)处理NCI-H929细胞,并通过流式细胞术评估细胞凋亡。SP-3164在72小时后诱导剂量依赖性早期和晚期细胞凋亡,而SP-3165未诱导细胞凋亡。在NCI-H929小鼠异种移植模型中评估SP-3164的体内活性并与SP-3165、LEN和POM进行比较。SP-3164作为单一药物显示出显着的TGI,而SP-3165似乎支持肿瘤生长。LEN和POM表现出最弱的TGI。与POM+DEX联合使用相比,SP-3164与地塞米松(DEX)联合使用时,TGI有所改善。
同时,SP-3164可以有效降解Ikaros和Aiolos(I/A),在临床前NHL模型中显示出令人信服的活性。

流式细胞术在NVP-DKY709 PD研究中的应用
NVP-DKY709,一种IKZF2(Helios)转录因子的选择性降解物,不降解IKZF1/3。研究表明,NVP-DKY709在体外可降低人调节性T细胞的抑制作用,并使耗竭Teff分泌细胞因子,降低小鼠的肿瘤生长,并降解猴子和人体内的IKZF2。
① 通过流式细胞术体外评估DKY709对T细胞和Tregs细胞的影响。
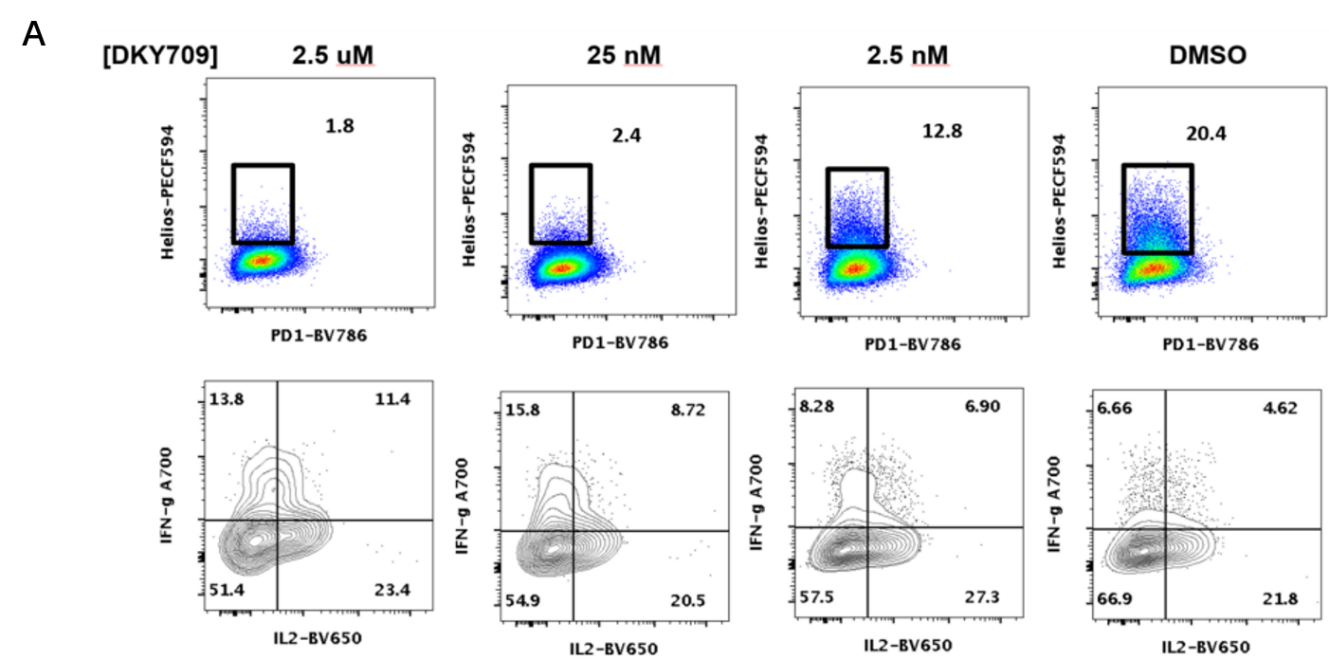
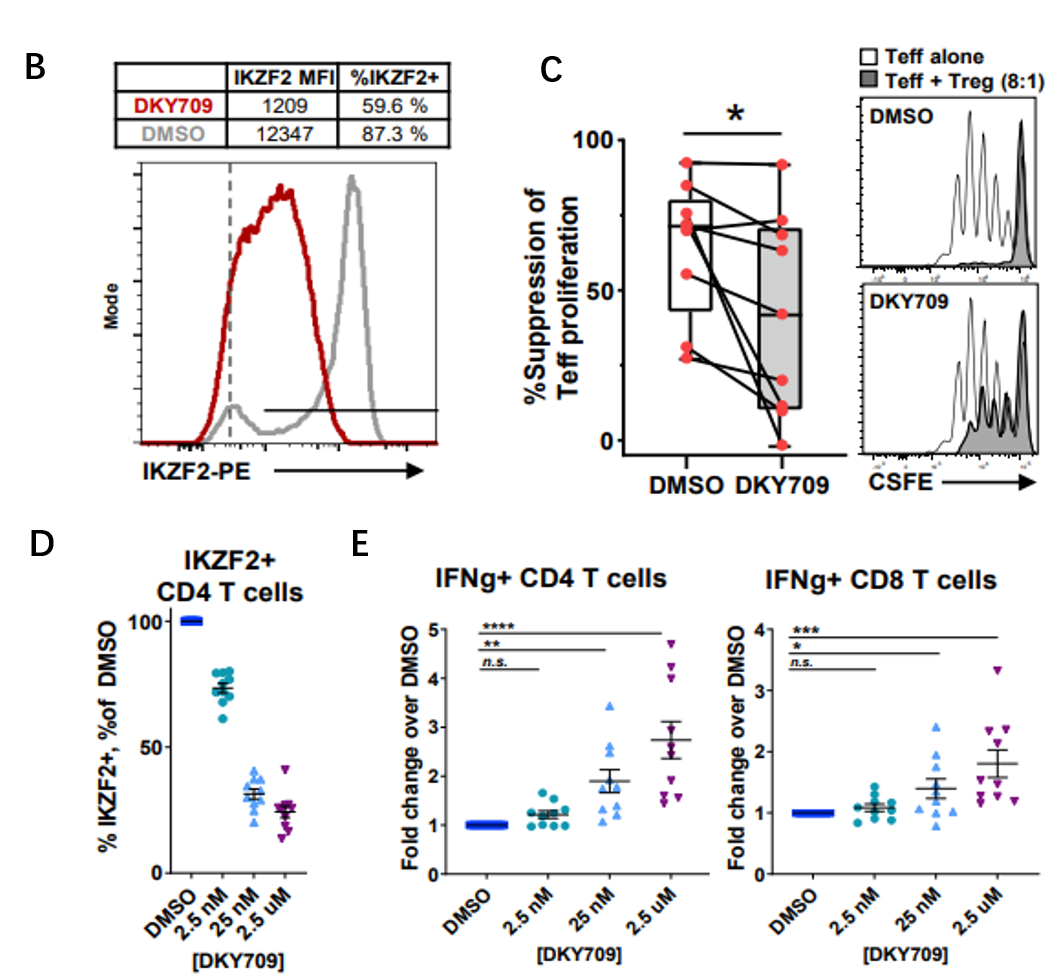
图5 A.D&E的圈门策略; B.人原代Treg细胞体外孵育10μM DKY709或DMSO的数据,包括%IKZF2+和IKZF2 MFI;C.人原代Treg细胞在DKY709作用下会扩增,并抑制Teff细胞增殖;D&E不同浓度DKY709作用于重复TCR刺激诱导的功能失调的Teff细胞,IKZF2+以及IL-2和IFN-γ水平的变化
② 通过流式细胞术评估小鼠和食蟹猴给药DKY709对T细胞和Tregs细胞的影响。
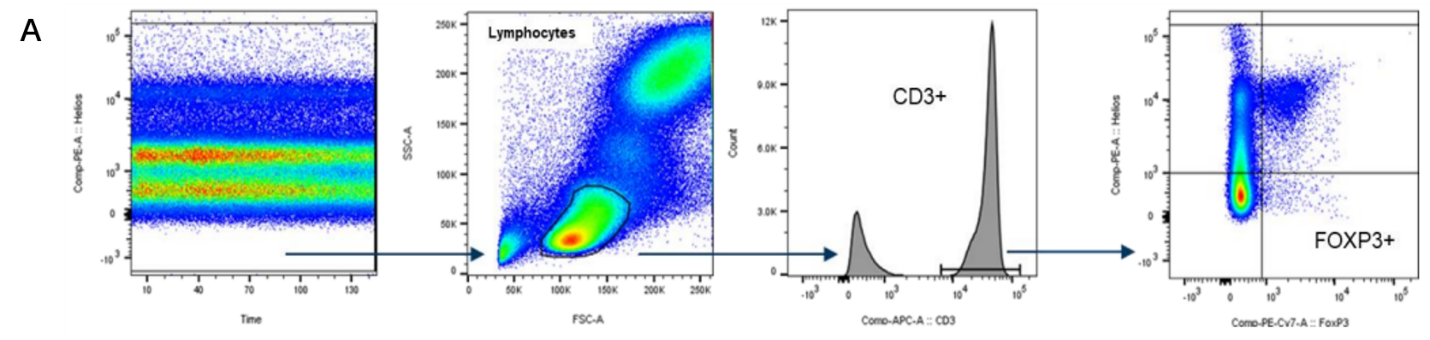
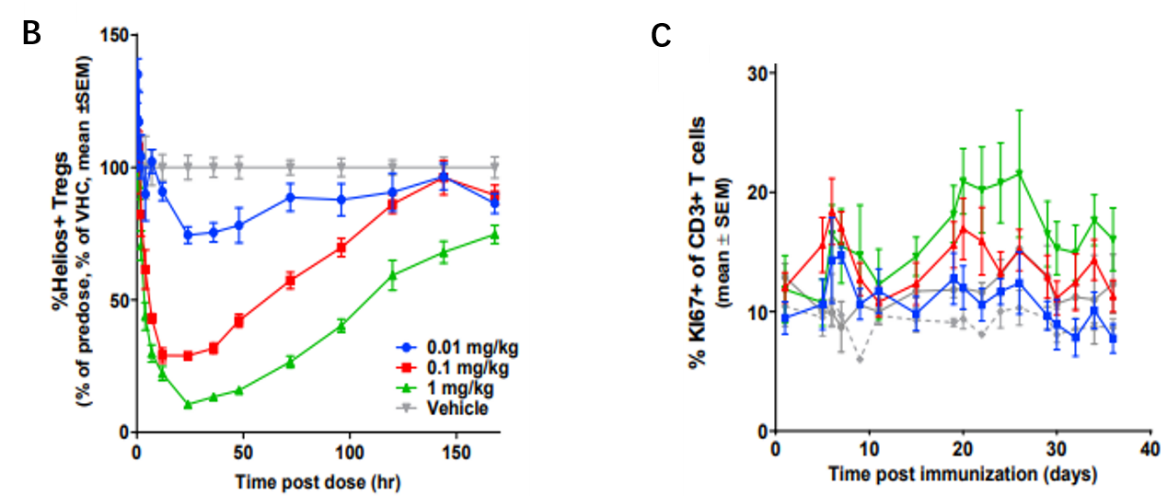
图6 A. B的圈门策略;B. 通过流式细胞术测定单次口服DKY709后食蟹猴血液中Treg细胞中IKZF2水平;C. 每日给予KLH免疫的食蟹猴指定剂量的DKY709后,通过流式细胞术测定外周血CD3+细胞中Ki67的表达水平来评估外周血T细胞的增殖能力
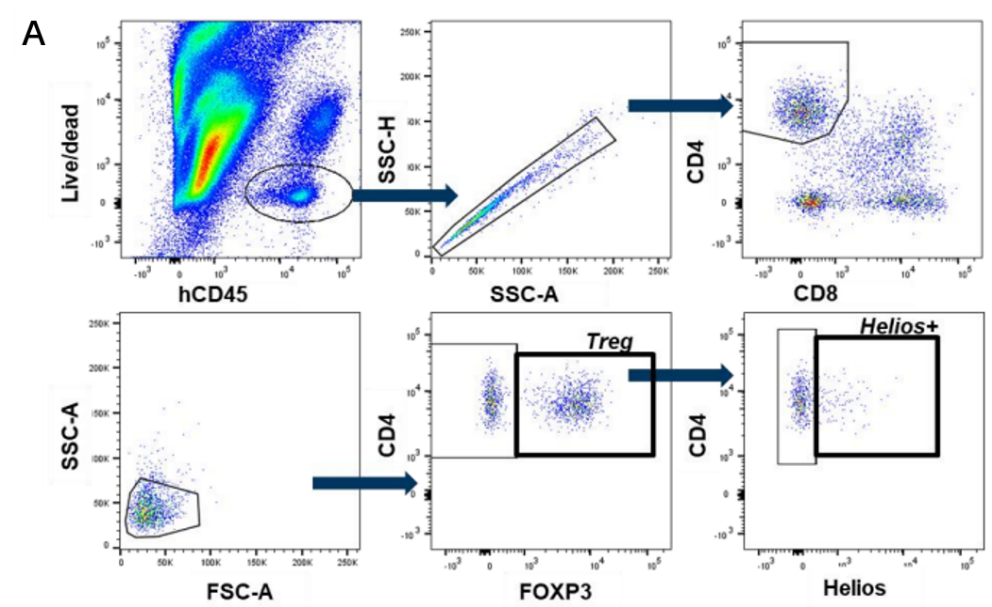
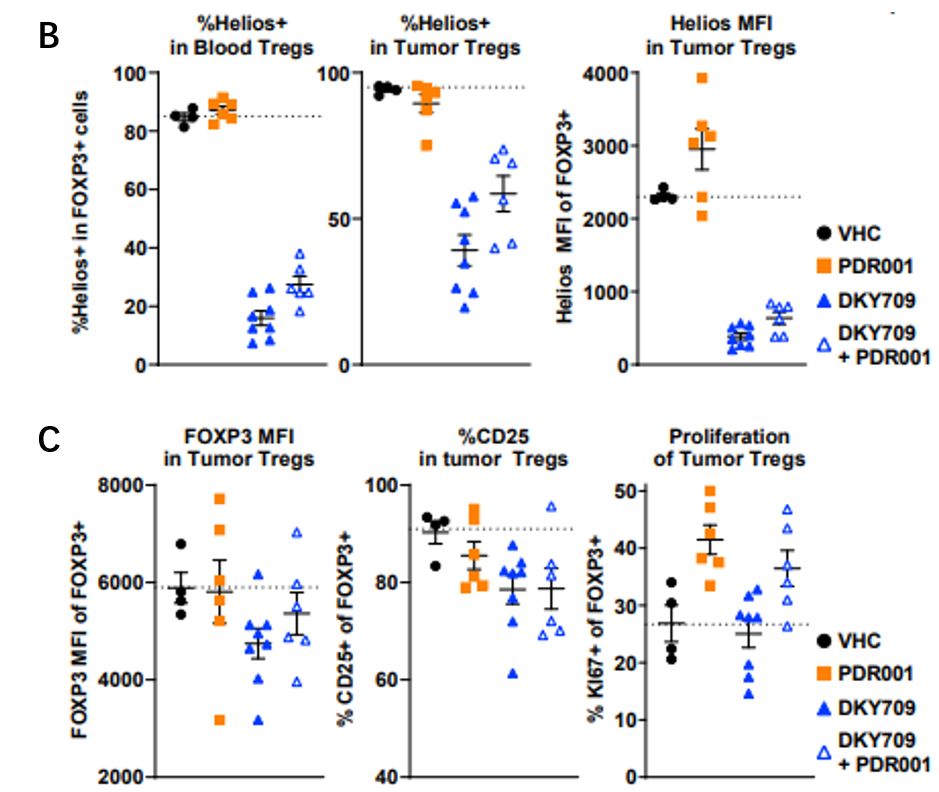
图7 A. B&C的圈门策略;B. 人源化小鼠MDA-MB-231肿瘤移植模型中IKZF2在原代Foxp3+ Treg细胞中的体内降解,血液(左)和肿瘤浸润(右);C. 通过流式细胞术评估DKY709和PD1阻断治疗对肿瘤浸润性Treg细胞Foxp3 MFI和CD25表达和增殖的影响
③ 通过流式细胞术评估临床DKY709药效
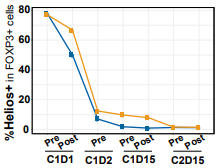
图8 通过流式细胞术评估两例在指定时间内每天接受20mg DKY709患者外周血Tregs中IKZF2的水平

流式细胞术在ARCC-29 PD研究中的应用
ARCC-29是一种蛋白水解靶向嵌合体(PROTAC)分子,它通过蛋白酶体诱导BET(BRD4/3/2)蛋白降解。ARCC-29 在几种人类恶性细胞系和体内啮齿动物异种移植肿瘤中降解BRD4。在前列腺(22Rv1)、DLBCL(SU-DHL-6)和卵巢(A2780)肿瘤的小鼠异种移植模型中,该分子表现出很强的PK/PD/疗效关系。从患者身上获取肿瘤组织通常需要侵入性操作,并且可能无法获得。已有相关研究开发了一种使用替代组织的检测方法来评估PROTAC的作用机制,这些机制可以应用于临床,通过流式细胞术来定量评估外周血单核细胞(PBMC)各亚群中BRD4的水平。将冷冻或新鲜的人PBMC与ARCC-29离体培养6小时,固定并透化以进行细胞内BRD4染色,并在门控淋巴细胞中定量BRD4水平。ARCC-29在四个新鲜PBMC样品中将BRD4水平降低到对照的13%、10%、16%和9%,在六个冷冻PBMC样品中降低到10%、9%、11%、6%、8%和35%,与BRD4抑制剂OTX-015作用PBMC显示出相似或更强的抑制作用。流式细胞术检测PBMC为治疗前和治疗后的患者样本在临床上确认PROTAC的作用机制提供了潜在的替代方法。
PART 03
熙宁生物|精翰生物冻存全血专利助力分子胶和PROTAC药物临床PD检测
表1 FACS熙宁|精翰部分冻存稳定性数据展示
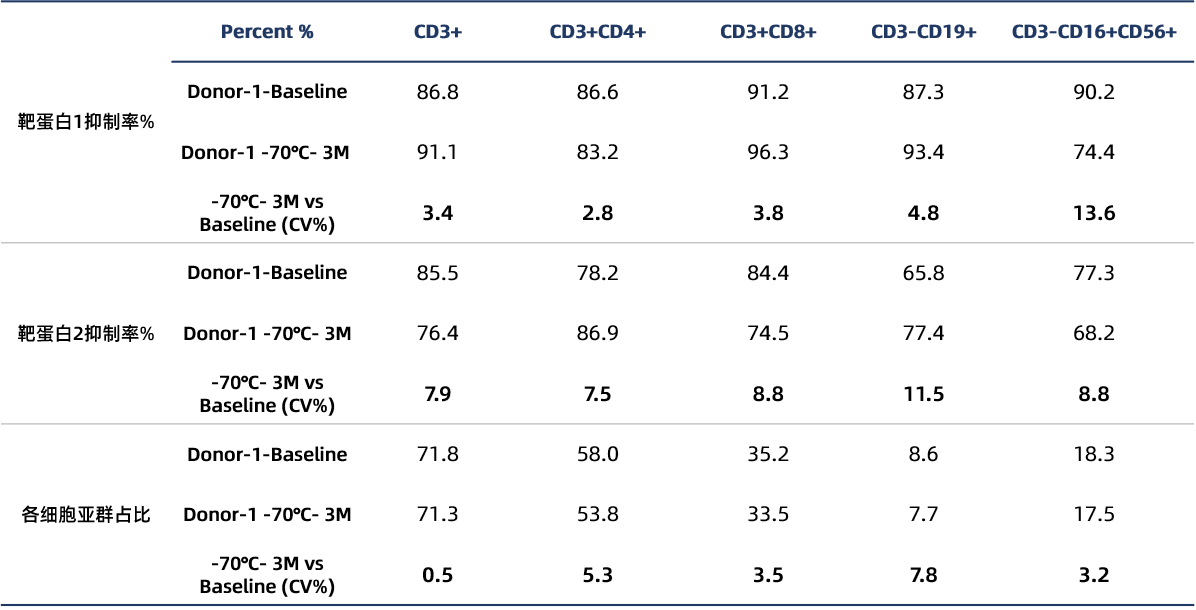
冻存稳定性总结:
➢
-70℃冻存3个月,与基线相比,各亚群的靶蛋白1的抑制率%CV范围为:2.8%-13.6%。
➢
-70℃冻存3个月,与基线相比,各亚群的靶蛋白2的抑制率%CV范围为:7.5%-11.5%。
➢
-70℃冻存3个月,与基线相比,各亚群的占比%CV范围为:0.5%-7.8%。
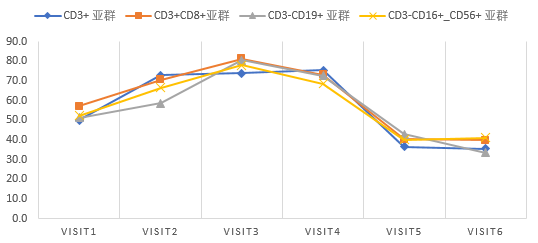
图9 各细胞亚群抑制率(%)
FACS熙宁|精翰部分临床样品数据展示。分别在给药前D1-Pre,给药后各时间点检测全血样品中各细胞亚群靶蛋白抑制率,给药后有明显抑制
表2 FACS检测胞内/核内因子相关案例经验

熙宁|精翰生物流式平台,不断进行技术迭代,开发创新。针对流式分析血液样品稳定性时间短,需要及时运输;或者是需要在临床中心分离PBMC,耗时耗力,效果不佳等行业痛点,开发了全血直接冻存技术,目前已获得国家专利授权,提高了各方的运营效率,减小了数据的批间差异,提高了数据的可比性,为行业创造了价值,受到了来自申办方和临床试验中心的一致欢迎和好评;为国际多中心临床样品的流式检测,提供了解决方案。基于全血冻存技术,熙宁|精翰开展了一系列的应用拓展,包括但不限于:
基于冻存全血的靶点降解检测
稳定性预计至少3个月
基于冻存全血的淋巴细胞亚群比例检测
稳定性可达12个月;
基于冻存全血的淋巴细胞亚群比例和
绝对计数检测
稳定性预计可达至少6个月
基于冻存全血的受体占位检测
(受体占位靶点包括PD-1,PD-L1, TIGIT, PVRIG, CD19,CD20, CD33, CD38, CD39, CD47, CD73等)
稳定性可达6-12个月
熙宁|精翰流式细胞团队由30余名经验丰富的人员组成,配备BD流式细胞仪、Beckman流式细胞仪、Cytek光谱流式细胞仪等仪器和设备,支持过包括抗体类药物、基因与细胞治疗药物、小分子创新药等各类新药的流式分析检测,其中抗体药物>40个,基因与细胞治疗药物>50 个,小分子创新药>20 个,临床试验>100 个,更是支持国内第一款I 类新药的CAR-T产品- 药明巨诺倍诺达®(瑞基奥仑赛注射液)的样本检测分析工作。平台能够支持包括免疫细胞亚群分型检测,细胞治疗产品的PK/PD 分析,抗体药物的受体占位分析,PD指标蛋白磷酸化、甲基化、乙酰化检测,胞内因子检测等。尤其在血液肿瘤淋巴细胞亚群检测中具有大量的实战经验,欢迎咨询沟通。
参考文献:
[1] Zhao L, Zhao J, Zhong K, et al. Targeted protein degradation: mechanisms, strategies and application[J]. Signal Transduction and Targeted Therapy, 2022, 7(1): 113.
[2] Sasso J M, Tenchov R, Wang D S, et al. Molecular glues: The adhesive connecting targeted protein degradation to the clinic[J]. Biochemistry, 2022, 62(3): 601-623.
[3] LIU S, DOU S, WANG J, et al. Market Analysis and Countermeasures for Targeted Protein Degradation Drugs[J]. China Biotechnology, 2023, 43(2/3): 190-200.
[4] Duncan, Aundrietta D., et al. "SP-3164, a novel molecular glue degrader with activity in preclinical models of multiple myeloma." Cancer Research 83.7_Supplement (2023): 6253-6253.
[5] Santiesteban D, Duncan A D, Mirza N Q, et al. P1241: A NOVEL CEREBLON-BINDING MOLECULAR GLUE, SP-3164, SHOWS PRECLINICAL ACTIVITY IN NON-HODGKIN LYMPHOMAS[J]. HemaSphere, 2023, 7(S3): e95971dd.
[6] Bonazzi S, d’Hennezel E, Beckwith R E J, et al. Discovery and characterization of a selective IKZF2 glue degrader for cancer immunotherapy[J]. Cell Chemical Biology, 2023, 30(3): 235-247. e12.
[7] Solomon J, Bonazzi S, d'Hennezel E, et al. Targeted degradation of IKZF2 for cancer immunotherapy[J]. 2022.
[8] Gough S M, Raina K, Gordon D, et al. IHC and flow cytometry quantifies BRD4 levels in surrogate tissues after ex-vivo and in-vivo dosing with a BRD4 degrading PROTAC[J]. Cancer Research, 2017, 77(13_Supplement): 5076-5076.