



PD-L1不同检测抗体互用性比较
熙宁小课-第122期 | PD-L1免疫组化检测抗体怎么选?(上) 主要介绍了PD-L1免疫组化检测5种常见抗体的应用,我们会发现同一适应症不同药物对应的PD-L1检测试剂盒不同,与疗效相关的PD⁃L1阳性判读阈值亦不相同,那么不同抗体间检测的结果是否可以互用,阳性判读阈值是否可以互用?
针对这个问题,目前已有较多的研究,比较有影响力的是国际肺癌研究协会(International Association for the Study of Lung Cancer, IASLC)牵头发起的蓝印计划,蓝印计划1期研究中使用四种PD-L1 抗体(22C3、28-8、SP142和SP263)对总共38例NSCLC肿瘤标本进行了染色,三位病理医生独立评估了染色结果,判读阈值采用所有抗体对应cut-off值,28-8和22C3抗体为TC≥1%染色,SP 263抗体为TC≥25%染色,SP142抗体为TC≥1%染色或PD-L1阳性IC(TC1/IC1)面积占比≥1%。
PART 01
不同抗体染色一致性研究
分析比较表明,当使用22C3、28-8和SP263抗体时,PD-L1染色的肿瘤细胞的百分比一致率较高,而SP142抗体总体上显示出肿瘤细胞膜染色较弱、阳性肿瘤细胞较少、敏感性较低的结果,与另外三种抗体相比存在偏离。不同抗体免疫细胞染色结果差异性高于肿瘤细胞染色结果(图1)。
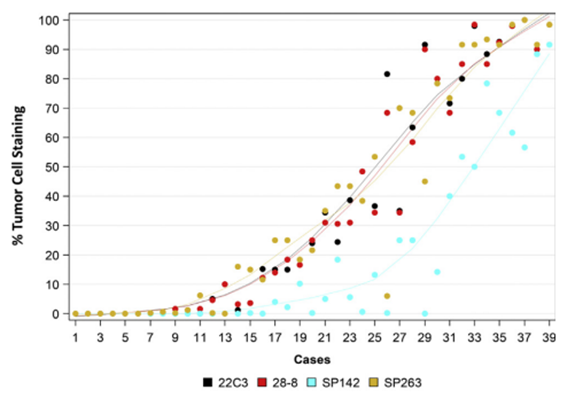
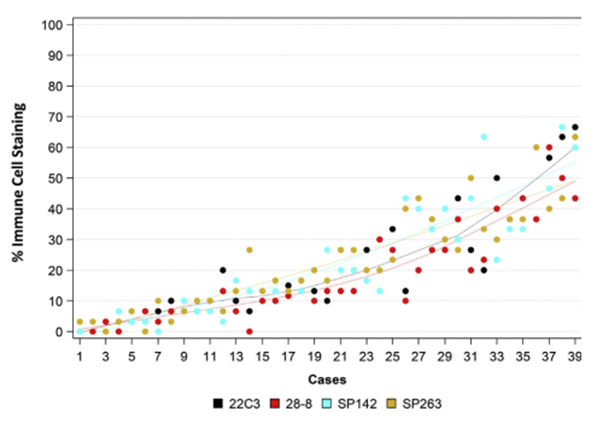
图1每种抗体测定的肿瘤细胞和免疫细胞染色百分比的分析比较[6]
PART 02
基于不同抗体cut-off值患者分类一致性研究
通过比较不同抗体检测结果阳性患者分类,来评估临床诊断的一致性。在38例样本中,50%(19/38)的样本在四种抗体的检测中均显示高于其cut-off值,13.1%(5/38)的样本在四种抗体的检测中均显示低于其cut-off值,而36.9%(14/38)的样本在四种抗体的检测中显示出不一致的分类结果(图2)。其中SP263抗体检测结果显示高于阈值的样本较少,因为与28-8和22C3的1%阈值相比,25%的TC染色阈值更高。SP142检测染色的肿瘤细胞较少,因此肿瘤细胞评分高于阈值的样本较少,但由于额外评估免疫细胞染色,又有6例样本高于阈值,阳性率得到了补偿(图2)。
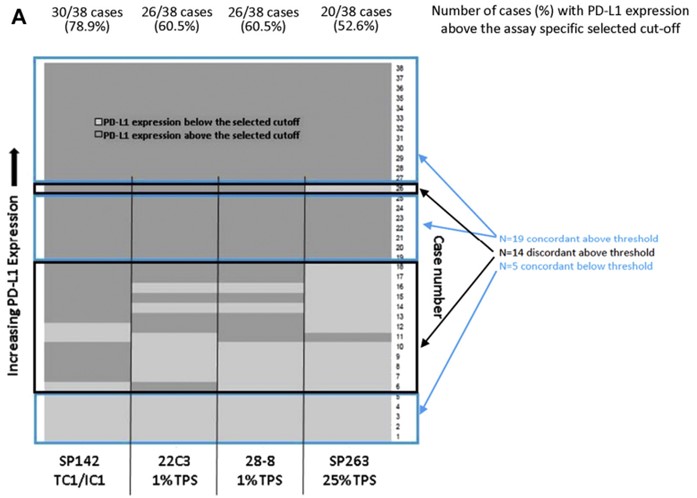
图2 高于或低于临床分析阈值的病例比较[6]
注:展示了用四种PD-L1 抗体检测结果分类的一致率,浅灰色表示低于阈值,深灰色表示高于阈值。
PART 03
不同抗体cut-off值互用性研究
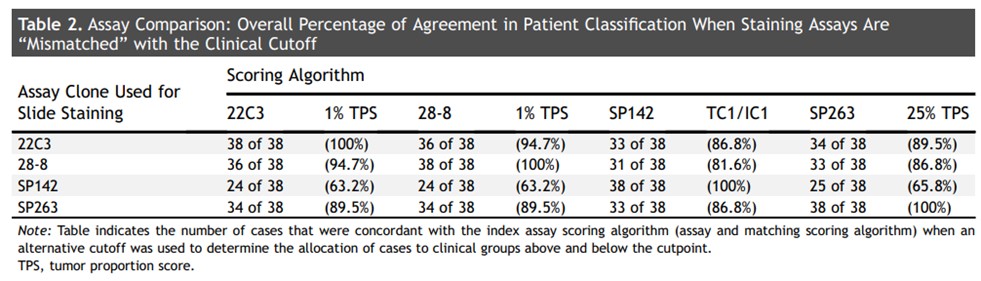
另外也对不同抗体所采用的cut-off值进行了互用性研究,22C3 采用28-8 或SP263对应的 cut-off值,28-8采用22C3或SP263对应的cut-off值,及SP263采用22C3或28-8对应的 cut-off值进行判读,结果表明,不同组合下所判读结果与自身抗体cut-off判读结果的一致率为86.8%~94.7%;SP142采用22C3、28-8和SP263的cut-off判读,一致率仅为63.2%~65.8%;22C3、28-8 和SP263采用SP142判读标准,一致率仅为81.6%~86.8%。尽管研究中22C3、28-8和SP263染色相似,但22C3采用28-8或SP263对应的cut-off值,28-8采用22C3或SP263对应的cut-off值,以及SP263采用22C3或 28-8对应的cut-off值判读仍存在5.3%~13.2%的不同,所以采用不同的判读结果可能直接影响治疗方案的选择(表1)。
表1 分析比较:当染色抗体与临床cut-off值“不匹配”时,
患者分类的总体一致率[6]
PART 04
小结
随后的蓝印计划2期研究加入了大家熟悉的73-10检测抗体,与22C3和28-8一样,73-10抗体为阿维鲁单抗的诊断试剂。蓝印计划2期研究也扩大了样本量、样本类型及病理医生的团队,以便更好的评估真实世界临床样本结果,该研究在81例肺癌样本中使用22C3、28-8、SP142、SP263及73-10抗体进行检测, 2期研究确认了1期的研究结论:28-8、22C3和SP263三种抗体检测肿瘤细胞具有一致性,SP142 检出阳性细胞较少,敏感性低,新加入的73-10抗体相比于其他抗体可检出更多的阳性细胞,表现出更高的灵敏度(图3)。
多项研究表明,E1L3N与22C3、28-8、SP263抗体有着良好的一致性 [8-13],虽然各项研究结果表明,E1L3N、22C3、28-8和SP263一致性较高,但目前的指南仍然认为,尚缺乏足够的前瞻性临床研究证据支持抗体间检测结果互用的可行性,仍建议根据不同的抗PD-1或PD-L1药物选择其对应的PD-L1检测抗体克隆及相应的检测平台。
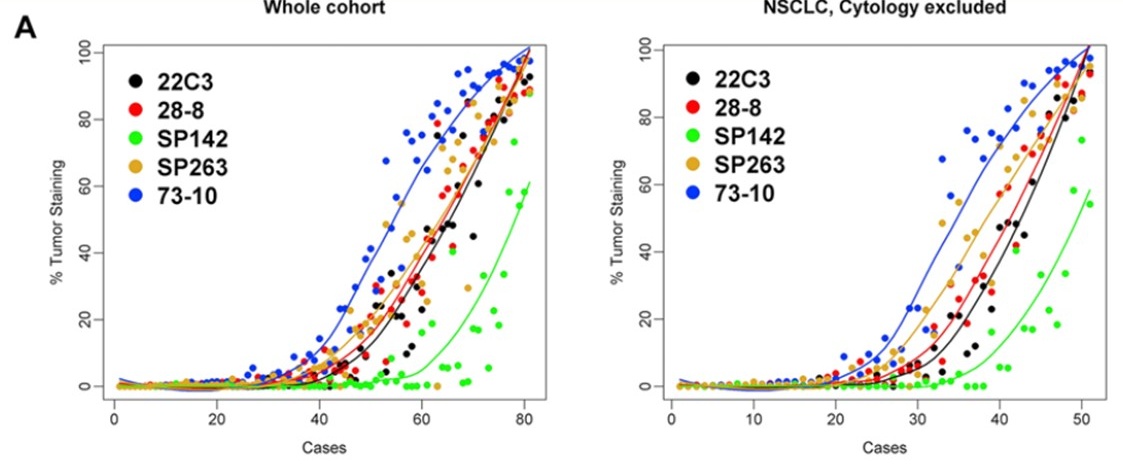
图3 PD-L1在5种抗体中的染色结果比较[7]
熙宁生物|精翰生物PD-L1检测服务
基于PD-L1抗体间检测结果互用可行性研究,熙宁生物|精翰生物建立了PD-L1检测的多种抗体平台,包括22C3、28-8、SP263、E1L3N四种主流的灵敏度、特异性、一致性表现优异的抗体。熙宁生物|精翰生物紧跟最新药物研发需求,致力于为申办方提供全面的PD-L1表达检测平台。熙宁生物|精翰生物免疫组化实验室拥有BenchMark Ultra,Dako Autostainer Link 48,Leica Bond III等PD-L1不同抗体适配的全自动免疫组化染色平台,已建立了PD-L1检测标准化操作流程,成功完成22C3、28-8、SP263、E1L3N 4种抗体检测方法学开发及性能验证,可支持申办方根据对标药物对应的诊断抗体按需选择。
4种抗体22C3、28-8、SP263、E1L3N部分检测数据展示:
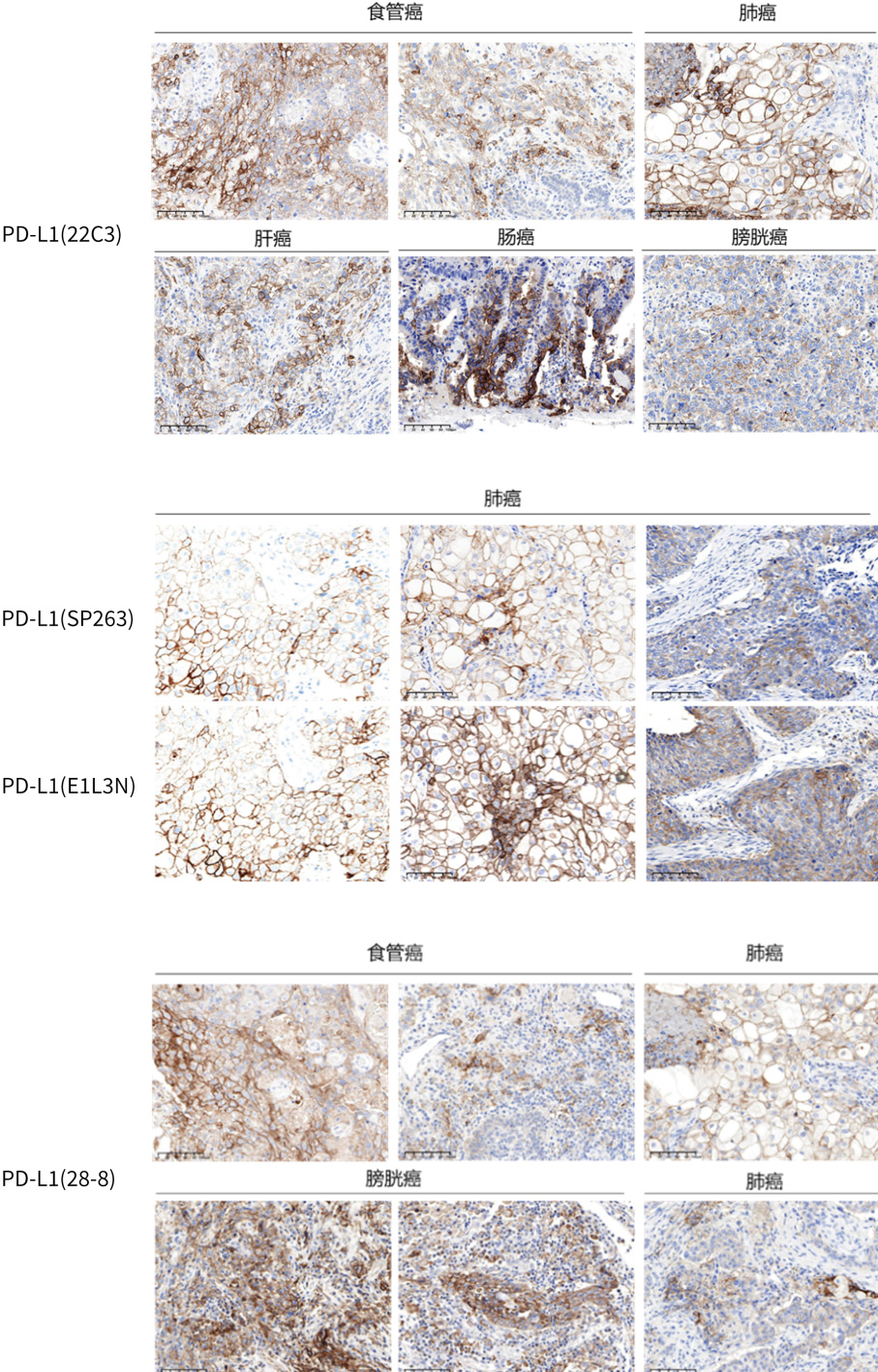
熙宁生物|精翰生物免疫组化平台多次高分通过国内外权威机构举办的室间质评,全流程标准化操作与质量控制也获得权威机构的充分认可,能够为客户提供精准优质的技术服务和严谨细致的质量保证。

PD-1/PD-L1免疫治疗患者入排检测服务
免疫治疗中针对EGFR及ALK阴性非小细胞肺癌患者入排检测,熙宁生物|精翰生物NGS和PCR平台有多款产品可以支持,针对HER2阴性胃癌和三阴性乳腺癌患者入排检测,熙宁生物|精翰生物的IHC、FISH和CISH平台也可以很好地满足该检测需求,具体的样本检测周期亦可结合申办方需求进行合理调整。
熙宁生物 | 精翰生物病理检测及CDx开发
熙宁生物|精翰生物免疫组化实验室拥有BenchMark Ultra,Dako Autostainer Link 48,Leica Bond III等国际公认的全自动免疫组化染色平台,遵从CAP和GCP体系要求,按照“合规、精准、伴随诊断”的理念,成功完成包括PD-L1、Claudin18.2、HER2、HER3、TROP-2、dMMR、TIM-3、MSLN、B7H3等超200种靶标的免疫组化方法开发,且多种方法已获得NordiQC、CAP、CCPI等国内外权威机构的认可。
除上述提到的免疫组化检测,熙宁生物|精翰生物免疫组化实验室还可支持H&E染色,免疫组化(单染,双染),mIHC,FISH,特殊染色等技术服务,满足临床试验检测需求。
对于客户的伴随诊断需求,我们已筛选出了多株具有伴随诊断开发价值的单克隆抗体并完成了前期的试剂盒开发,可为广大药企客户提供伴随诊断试剂盒开发服务,欢迎致电咨询。
部分IHC结果展示
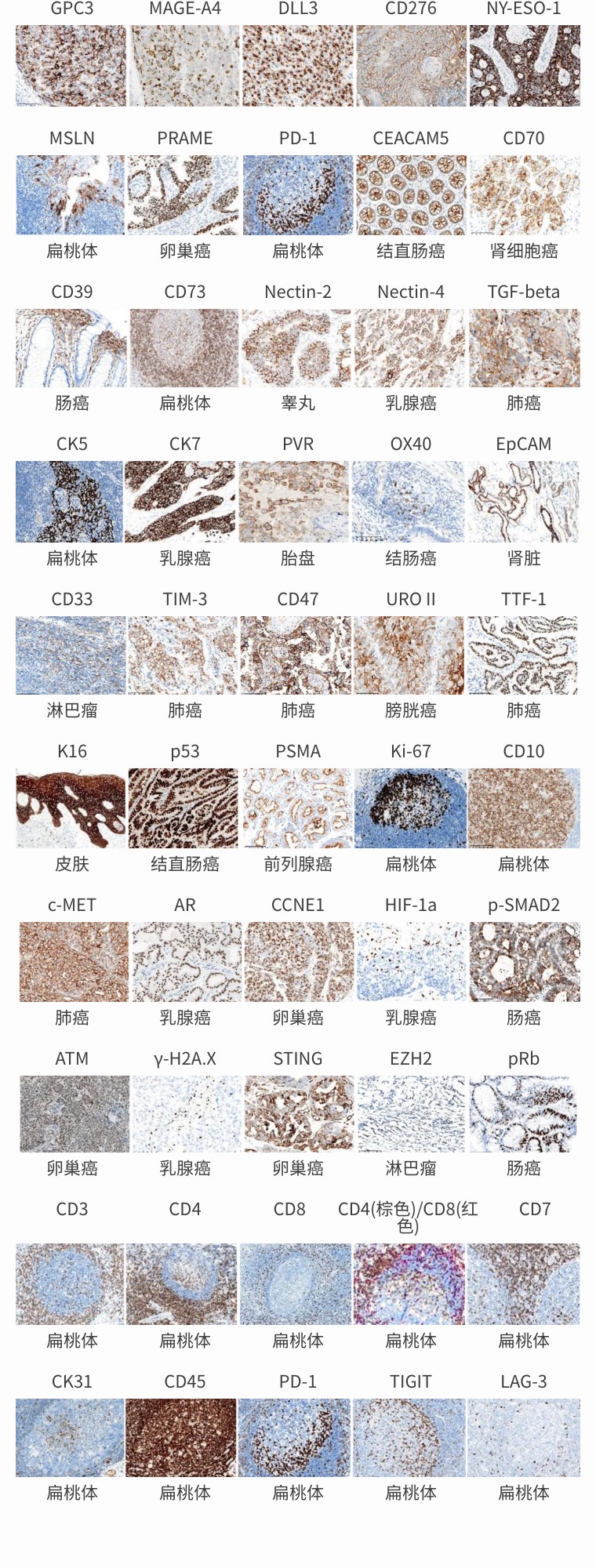
参考文献
[1] 实体肿瘤PD-L1免疫组织化学检测专家共识(2021版)
[2] Kang SP, Gergich K, Lubiniecki GM, et al. Pembrolizumab KEYNOTE-001: an adaptive study leading to accelerated approval for two indications and a companion diagnostic. Ann Oncol. 2017;28(6):1388-1398. doi:10.1093/annonc/mdx076
[3] Downs-Canner S, Mittendorf EA. Preoperative Immunotherapy Combined with Chemotherapy for Triple-Negative Breast Cancer: Perspective on the KEYNOTE-522 Study [published correction appears in Ann Surg Oncol. 2023 Apr 4;:]. Ann Surg Oncol. 2023;30(6):3166-3169. doi:10.1245/s10434-023-13267-z
[4] Lu S, Fang J, Wang Z, et al. Primary results from the China Cohort of IMpower132: atezolizumab (atezo) + carboplatin (carbo) or cisplatin (cis) + pemetrexed (pem) as first-line therapy in advanced NSCLC[EB/OL]. ELCC 2021, abstract 102P.
[5] 102P - Primary results from the China Cohort of IMpower132: atezolizumab (atezo) + carboplatin (carbo) or cisplatin (cis) + pemetrexed (pem) as first-line therapy in advanced NSCLC
[6] Hirsch FR, McElhinny A, Stanforth D, et al. PD-L1 Immunohistochemistry Assays for Lung Cancer: Results from Phase 1 of the Blueprint PD-L1 IHC Assay Comparison Project. J Thorac Oncol. 2017;12(2):208-222. doi:10.1016/j.jtho.2016.11.2228
[7] Tsao MS, Kerr KM, Kockx M, et al. PD-L1 Immunohistochemistry Comparability Study in Real-Life Clinical Samples: Results of Blueprint Phase 2 Project. J Thorac Oncol. 2018;13(9):1302-1311. doi:10.1016/j.jtho.2018.05.013
[8] Ahn S, Lee Y, Kim JW, et al. Programmed cell death ligand-1 (PD-L1) expression in extrahepatic biliary tract cancers: a comparative study using 22C3, SP263 and E1L3N anti-PD-L1 antibodies. Histopathology. 2019;75(4):526-536. doi:10.1111/his.13901
[9] Munari E, Zamboni G, Lunardi G, et al. PD-L1 expression in non-small cell lung cancer: evaluation of the diagnostic accuracy of a laboratory-developed test using clone E1L3N in comparison with 22C3 and SP263 assays. Hum Pathol. 2019;90:54-59. doi:10.1016/j.humpath.2019.05.003
[10] Zhang W, Cao Z, Gao C, et al. High concordance of programmed death-ligand 1 expression with immunohistochemistry detection between antibody clones 22C3 and E1L3N in non-small cell lung cancer biopsy samples. Transl Cancer Res. 2020;9(10):5819-5828. doi:10.21037/tcr-20-101
[11] Song L, Zeng L, Yan H, et al. Validation of E1L3N antibody for PD-L1 detection and prediction of pembrolizumab response in non-small-cell lung cancer. Commun Med (Lond). 2022;2(1):137. Published 2022 Nov 1. doi:10.1038/s43856-022-00206-4
[12] Smith J, Robida MD, Acosta K, et al. Quantitative and qualitative characterization of Two PD-L1 clones: SP263 and E1L3N. Diagn Pathol. 2016;11(1):44. Published 2016 May 18. doi:10.1186/s13000-016-0494-2
[13] Smith J, Robida MD, Acosta K, et al. Quantitative and qualitative characterization of Two PD-L1 clones: SP263 and E1L3N. Diagn Pathol. 2016;11(1):44. Published 2016 May 18. doi:10.1186/s13000-016-0494-2
[14] 中国非小细胞肺癌PD-L1表达检测临床病理专家共识[J]. 中华肿瘤杂志,2020,42(7):513-521.
[15] Zhou YJ, Li G, Wang J, et al. PD-L1: expression regulation. Blood Sci. 2023;5(2):77-91. Published 2023 Jan 13. doi:10.1097/BS9.0000000000000149
[16] Patel SP, Kurzrock R. PD-L1 Expression as a Predictive Biomarker in Cancer Immunotherapy. Mol Cancer Ther. 2015;14(4):847-856. doi:10.1158/1535-7163.MCT-14-0983
[17] Tsao MS, Kerr KM, Kockx M, et al. PD-L1 Immunohistochemistry Comparability Study in Real-Life Clinical Samples: Results of Blueprint Phase 2 Project. J Thorac Oncol. 2018;13(9):1302-1311. doi:10.1016/j.jtho.2018.05.013