



PART.1
DDR与合成致死
DNA损伤应答(DNA damage response,DDR)在维持基因组稳定方面起到重要作用。在外界压力(UV辐射、电离辐射、化学物质等)或内源性因子(复制错误、细胞代谢、氧化应激等)的刺激下,细胞DNA受到损伤,最终可能导致DNA单链或双链断裂[1]。为了修复DNA的损伤,细胞内存在多种复杂、精确的修复途径来维持基因组稳定和细胞存活,包括非同源末端连接(non-homologous-end-joining,NHEJ)、同源重组(homologous recombination,HR)、错配修复(mismatch repair,MMR)、核苷酸切除修复(nucleotide excision repair,NER)、碱基切除修复(base excision repair,BER)、跨损伤修复(translesion synthesis,TLS)、链间交联(interstrand crosslinks,ICL)[2]。
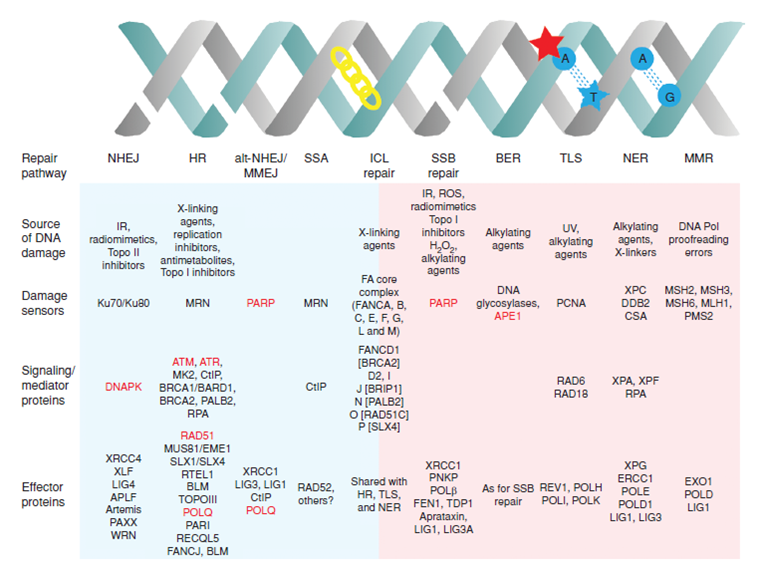
图1 主要DNA修复途径的关键传感器、信号和效应蛋白[2]
相比于正常细胞,肿瘤细胞通常在DNA损伤修复通路中存在缺陷,使得快速增殖的肿瘤细胞更加依赖于特定的某一修复途径,因此肿瘤细胞对特定的DDR抑制更加敏感[3]。DDR抑制剂能够以“合成致死”方式起作用,选择性地杀死癌细胞,同时保留正常细胞,提供了一种可以区分肿瘤细胞和正常细胞的肿瘤靶向治疗策略[3]。

图2 合成致死的作用机制
注:单独抑制或缺乏A或B基因不影响细胞存活,而在肿瘤细胞中抑制或缺乏这两种基因(A和B)会导致细胞死亡[3]
DNA损伤修复过程涉及多种蛋白,如PARP,RAD51,ATM,ATR,CHK1,WEE1,PKMYT1,DNA-PK,POLQ和USP1等,这些蛋白活性和功能的异常通常与肿瘤相关。与此同时,这些蛋白也是合成致死领域研究的热门靶点。本文将于ATR抑制剂为例,简单介绍“合成致死”抑制剂的临床前和临床药效学评估。
PART.2
ATR的生理功能
ATR的主要作用是调节DNA复制和细胞周期检查点激活,特别是在S期内,以确保正常的细胞分裂,无论是在正常细胞过程还是在DNA损伤修复过程。ATR与ATRIP被招募到受阻或受损的DNA复制叉。通过解旋酶重塑其结构以防止切割,从而保护停滞的复制叉。然后通过HR因子,如BRCA2和PALB2,来促进DNA复制叉的修复。ATR还通过磷酸化CHK1的Ser-345以激活CHK1,随后活性CHK1介导细胞周期阻滞在S期或G2/M期,使DNA在细胞周期进程之前完成修复。[1, 3-5]
当ATR活性被抑制后,由于复制叉修复受损和积累,复制应激增加,这导致DSBs的大量形成,ATM和DNA-PKcs被激活,随后是其底物KAP1和H2AX的磷酸化以及DNA复制的不可逆崩溃,这被称为“复制灾难”。此外,抑制ATR活性同时也影响对细胞周期检查点的控制,在DNA损伤和基因组复制不完全的情况下迫使细胞过早进入有丝分裂,导致染色体断裂和有丝分裂细胞死亡[5]。
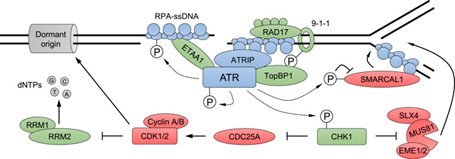
图3 S期检查点信号通路中ATR募集和激活模型[4]
抑制ATR活性既影响DNA检查点反应,又损害整体DSB修复,从而增强IR和DNA损伤药物治疗的疗效。“合成致死”原理也可以应用于ATR抑制,因为P53或ATM缺陷的肿瘤细胞只能依靠ATR参与的细胞周期检查点来修复DNA。选择性抑制ATR活性将导致肿瘤细胞中DNA缺陷的积累,从而引起有丝分裂灾难。这使得ATR成为解决放疗/化疗耐药性的一个潜在靶点。[1, 3]
PART.3
ATR抑制剂的药效学评估
目前已有多个ATR抑制剂处于临床II期研究,进展最快的化合物是AstraZeneca公司的Ceralasertib,该化合物针对三阴性乳腺癌或BRCA阳性乳腺癌的一项临床研究(NCT03150576)正处于II/III期阶段。
表1 部分ATR抑制剂的临床研究进展

对于ATR抑制剂的临床药效分析,更多的是选择ATR信号通路下游的效应蛋白作为药效学生物标志物。例如,Berzosertib的I期临床研究评价了5个患者肿瘤组织中pCHK1(S345)的含量,结果显示其中4个患者在药物治疗后pCHK1水平降低30%-90%(平均67%),表明Berzosertib有效抑制ATR活性,并且该结果支持RP2D选择(图4)[6]。临床前研究也在探索ATR抑制对p-ATR、p-KAP的影响,以期获得一些能够用于评价ATR抑制剂临床药效的指标[5, 7]。
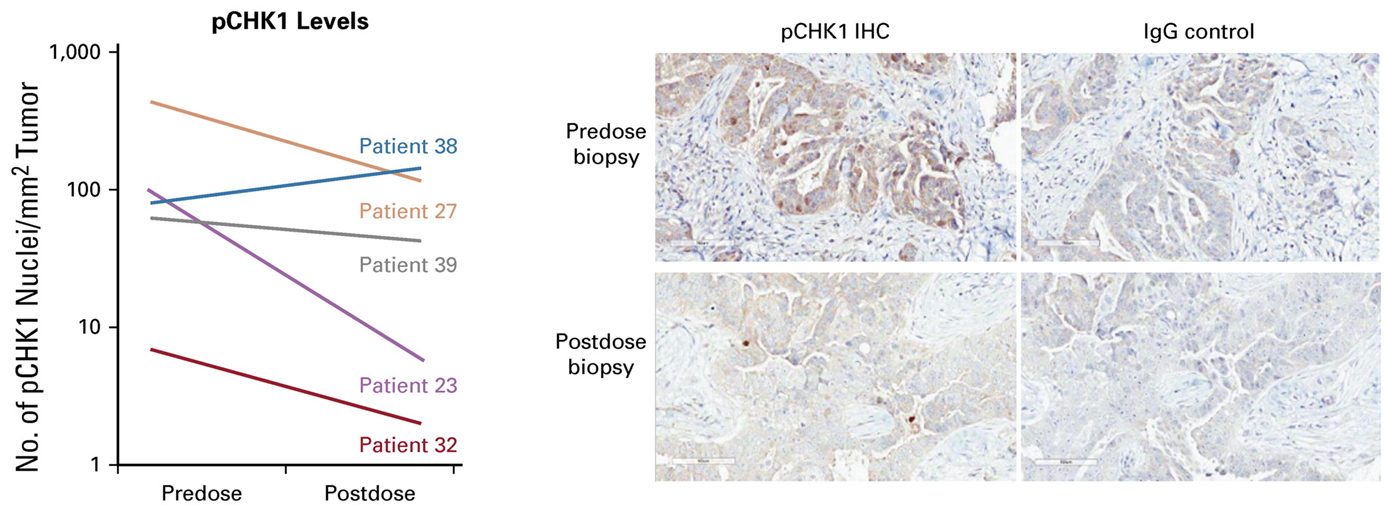
图4 Berzosertib的药效学生物标志物(pCHK1)评价[6]
值得注意的是,由于ATR与多个基因(如ATM、TP53)构成合成致死相互作用[8],所以在ATR抑制剂的临床研究中,通常会利用NGS或IHC检测患者基因的突变或缺失,以此为预测性生物标志物来筛选出最有可能从治疗中获益的优势人群[9-10]。例如,Ceralasertib的一项II临床研究(NCT03780608)显示(图5),ATM缺失和/或同源重组修复缺陷(Sig.HRD)的患者比ATM和同源重组修复功能正常患者的中位无进展生存期(PFS)明显更长(5.60个月vs 1.65个月;HR 0.13,95% CI 0.045 ~ 0.39;long-rank p < 0.001)[9]。

图5 预测性生物标志物(ATM、Sig.HRD)与临床药效相关性分析[9]
PART.4
小结
针对DDR相关靶点,熙宁生物|精翰生物可提供一体化、高效的临床生物分析服务。对于药效学生物标志物的检测,已建立多种生物标志物(pATM、pATR、pDNA-PKcs、γH2AX)的检测方法,同时也在继续开发其他药效学生物标志物(如pKAP、pCHK1/2、pCDK1等)的检测方法,可用于“合成致死”抑制剂的临床研究中有效性指标的探索。对于预测性生物标志物,熙宁生物|精翰生物的基因和免疫组化团队拥有丰富的项目经验,可根据客户需求,为临床试验人群的富集和患者入组提供预测性生物标志物的检测服务,包括基于NGS平台的全基因组筛查和基于IHC平台的组织病理筛查,欢迎大家后台留言咨询交流。
参考文献:
[1] Ronco C, et al. ATM, ATR, CHK1, CHK2 and WEE1 inhibitors in cancer and cancer stem cells. MedChemComm. 2016 Nov 30;8(2):295-319.
[2] Brown JS, et al. Targeting DNA Repair in Cancer: Beyond PARP Inhibitors. Cancer Discov. 2017 Jan;7(1):20-37.
[3] Cheng B, et al. Recent advances in DDR (DNA damage response) inhibitors for cancer therapy. Eur J Med Chem. 2022 Feb 15;230:114109.
[4] Blackford AN, Jackson SP. ATM, ATR, and DNA-PK: The Trinity at the Heart of the DNA Damage Response. Mol Cell. 2017 Jun 15;66(6):801-817.
[5] Roulston A, et al. RP-3500: A Novel, Potent, and Selective ATR Inhibitor that is Effective in Preclinical Models as a Monotherapy and in Combination with PARP Inhibitors. Mol Cancer Ther. 2022 Feb;21(2):245-256.
[6] Yap TA, et al. Phase I Trial of First-in-Class ATR Inhibitor M6620 (VX-970) as Monotherapy or in Combination With Carboplatin in Patients With Advanced Solid Tumors. J Clin Oncol. 2020 Sep 20;38(27):3195-3204.
[7] Harold J, et al. Elimusertib (BAY1895344), a novel ATR inhibitor, demonstrates in vivo activity in ATRX mutated models of uterine leiomyosarcoma. Gynecol Oncol. 2023 Jan;168:157-165.
[8] Kobayashi H, et al. Conceptual frameworks of synthetic lethality in clear cell carcinoma of the ovary. Biomed Rep. 2018 Aug;9(2):112-118.
[9] Yap TA, et al. Ceralasertib (AZD6738), an Oral ATR Kinase Inhibitor, in Combination with Carboplatin in Patients with Advanced Solid Tumors: A Phase I Study. Clin Cancer Res. 2021 Oct 1;27(19):5213-5224.
[10] Kwon M, et al. Phase II study of ceralasertib (AZD6738) in combination with durvalumab in patients with advanced gastric cancer. J Immunother Cancer. 2022 Jul;10(7):e005041.