



血液系统恶性肿瘤(HM)是一组包括白血病、淋巴瘤及多发性骨髓瘤等在内的造血系统疾病,具有恶性程度高、治疗复杂、预后差等特点。免疫组库测序在微小残留病灶(MRD)监测和克隆演变方面的研究逐渐增多,可辅助评估肿瘤治疗效果,并动态监测肿瘤的早期复发。
《中国多发性骨髓瘤诊治指南(2020年修订)》指出“微小残留病(Minimal Residual Disease, MRD)水平对MM预后有明显影响。”此外,在多篇临床指南与专家共识中均提出MRD检测可以辅助急性髓系白血病、多发性骨髓的临床治疗方案制定与患者的预后监测,具有重要的临床价值。
熙宁|精翰生物携手泛因医学,
开展血液瘤MRD检测
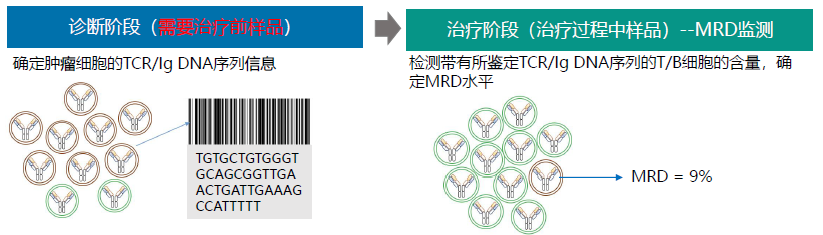
MRD是指恶性肿瘤经过治疗后体内残留的微量肿瘤细胞的状态。正常淋巴细胞未受任何刺激情况下,其基因重排是随机的,细胞表现为多家族和多克隆性,具有发挥各种细胞免疫作用的潜能。而在淋巴细胞白血病或淋巴瘤发生过程中,某一种或几种淋巴细胞发生异常增殖,这些异常增殖的淋巴细胞携带相同的TCR或BCR,导致TCR或Ig基因单克隆性表达,导致在淋巴结、外周血或者骨髓细胞中出现1个或2个主要淋巴细胞克隆。检测MRD能够准确获取体内残留肿瘤细胞的数量,有助于对疗效进行评估,提前发现复发趋势。
泛因医学NEO-MRD®检测通过精准地分析肿瘤细胞特异性标签,并跟踪定量患者治疗后的微小残留肿瘤细胞数量;同时评估肿瘤细胞是否发生了进化从而保证结果的准确性;还可以对机体免疫力进行监测。是国内首个获得欧盟CE认证的血液肿瘤MRD检测产品,NEO-具备检出率高、准确率高、自动化等特点,能够极大助力全球血液肿瘤微小残留病行业发展。
熙宁的血液瘤MRD检测经性能验证,确认灵敏度、特异性、精密度和稳定性等,均满足要求,性能可靠稳定,灵敏度可达10‐6,该检测项目的落地进一步强化公司检测分析一体化布局,可给申办方血液肿瘤药物临床研究开展提供完整的检测分析方案。
TCR/Ig编码基因是识别
不同T/B细胞的标志物
免疫组库(immunerepertoire, IR)是样品中TCR/Ig编码基因的总和。免疫组库测序(IR-seq)是对DNA或RNA样品中的TCR/Ig基因进行富集和测序。MRD的水平一般比较低,需要用敏感性和特异性都非常高的方法来进行检测。高灵敏度二代测序(NGS)MRD检测方法,其灵敏度可达1×10‐6,比标准MFC或PCR检测方法更灵敏。
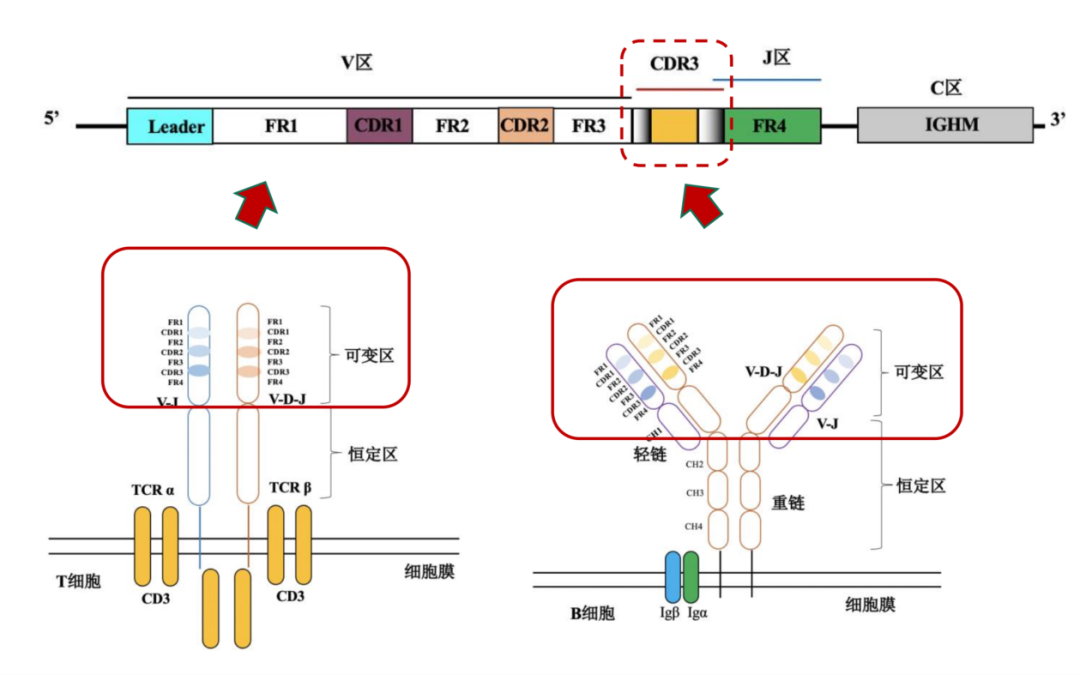
TCR为所有T细胞表面的特征性标志,以非共价键与CD3结合,形成TCR—CD3复合物。TCR的作用是识别抗原。TCR是由两条不同肽链构成的异二聚体,由α、β两条肽链组成,每条肽链又可分为可变区(V区),恒定区(C区),跨膜区和胞质区等几部分;其特点是胞质区很短。TCR分子属于免疫球蛋白超家族,其抗原特异性存在于V区;V区(Vα、Vβ)又各有三个高变区CDR1、CDR2、CDR3,其中以CDR3变异最大,直接决定了TCR的抗原结合特异性。在TCR识别MHC-抗原肽复合体时,CDR1、CDR2识别和结合MHC分子抗原结合槽的侧壁,而CDR3直接与抗原肽相结合。TCR分为两类:TCR1和TCR2;TCR1由γ和δ两条链组成,TCR2由α和β两条链组成。外周血中,90%-95%的T细胞表达TCR2;而且任一T细胞只表达TCR2和TCR1之一。
B细胞抗原受体(B-Cell Receptor, BCR)是一种位于B细胞表面的负责特异性识别及结合抗原的分子,其本质是一种膜表面免疫球蛋白(Membrane Lmmunoglobulin, MIg)。BCR具有抗原结合特异性,每个个体的BCR多样性高达5x10-13,构成容量巨大的BCR库,赋予个体识别各种抗原、产生特异性抗体的巨大潜能。在成熟B细胞表面,BCR总是和负责传递抗原刺激信号的Igα/Igβ(CD79a/b)异二聚体共同表达,形成BCR-Igα/Igβ复合体(BCR复合物)。编码重链基因的的染色体包括4种DNA元件(基因片段),分别是V、D、J、C。在人类B细胞中,V片段大约有50种,D片段大约有20种,J片段大约有6种,C片段大约有10种。而每个特异B细胞就是通过基因重排,选择每类片段中的一种,并将它们组合在一起,以组装成一个成熟的H-chain基因。
引物设计
准确灵敏的实验系统。该系统是基于准确无偏的Ig/TCR多重PCR实验系统进行肿瘤克隆鉴定和MRD检测的。在多重PCR中不同引物扩增效率的差异会带来扩增偏差,通过实验技术及数据处理算法的持续研发,该MRD检测方法将引物扩增效率优化至十分均衡,而均衡的扩增系统将带来MRD定量的高准确度和高灵敏度。
扩增多条受体链提高肿瘤细胞的检出率。实验体系包括IGH、IGK、IGL、TRB、TRD、TRG的受体链,可以准确的鉴定肿瘤细胞的标志序列,同时每条链还包括不同位置(FR1、FR2、FR3)的引物,可以有效的避免由于肿瘤细胞的突变引起的假阴性或定量不准确。
数据分析
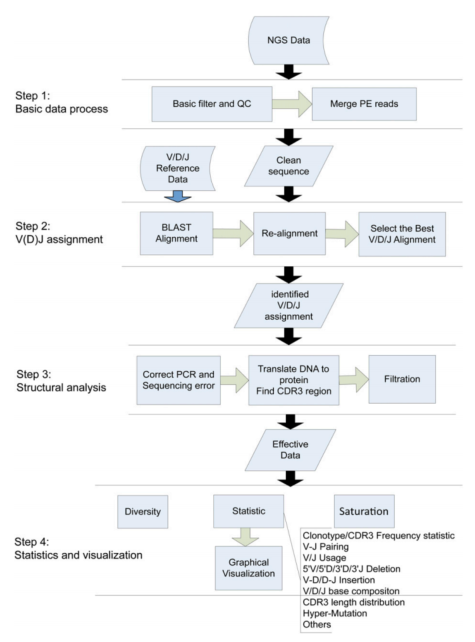
MRD数据分析流程示意图
MRD的数据分析流程基于IMonitor开发,包括免疫数据库比对、频率文件重构、测序错误纠正、生成excel结果、生成pdf报告。具体执行由图所示,将原始的双端测序数据合并,并分别与IMGT数据库的V/D/J参考序列进行比对,识别CDR3结构,统计克隆数。结果spike in序列估计样本总有核细胞数目,计算MRD值。根据已检测的数据库中是否存在受检者编号,决定该受检者为首次检测或追踪检测,针对首次检测的患者鉴定异常高频克隆并绘制异常高频克隆频数分布图,针对追踪检测患者绘制异常高频克隆追踪折线图,并生成pdf报告。
检测局限
(1)检测的灵敏度受样品体积和细胞数的直接影响,当MRD水平较低时,送检细胞数量太少可能会导致出现假阴性的结果。

(2)由于检测原理和方法的差异,不同方法检测的MRD水平可能有一定差异。
(3)样品类型、采样时间和位置的不同,检测结果可能会有所不同,尤其当MRD水平比较低的时候。
(4)样品污染、技术和生物学因素有可能导致检测结果出现假阳性和假阴性。
分析示例
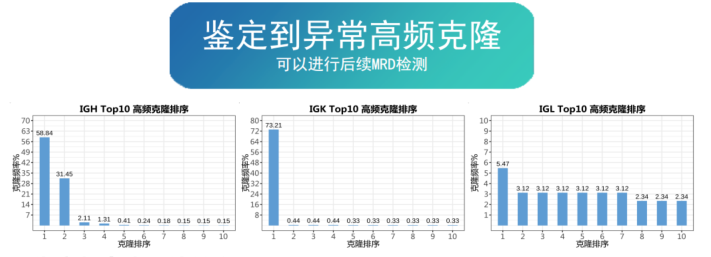
对上述患者进行首次克隆鉴定,根据图示结果可知,检测到3条异常高频克隆,包括2条IGH及1条IGK,克隆频率分别为58.85%、31.45%、72.21%,有核细胞占比均超过0.2%,呈断层式分布,符合异常高频克隆的鉴定标准。当该患者进行术后追踪检测时,其克隆鉴定/MRD分析结果如下:
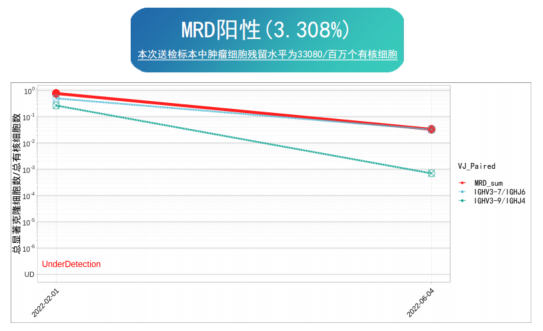
由图可知,送检标本中检测到肿瘤残留的克隆,残留水平为100万个有核细胞中有33080个肿瘤细胞,为临床诊断及肿瘤复发评估提供指导意义。
总结
熙宁生物(精翰生物)整体业务中涵盖了细胞治疗、基因治疗、单双抗和一些新型药物的临床检测。在细胞治疗业务中,绝大多数为血液瘤,因此,血液瘤MRD的检测方法的建立也是必不可少的。NEOMRD®可以评估MRD水平,同时监测是否有肿瘤克隆的演化克隆或新的高频克隆出现,评估由于原肿瘤克隆的演化克隆或亚克隆导致的复发风险,对疾病预后具有临床指导意义。
参考文献
中华医学会血液学分会实验诊断学组. 急性髓系白血病微小残留病检测与临床解读中国专家共识(2021年版) [J] . 中华血液学杂志, 2021, 42(11) : 889-897. DOI: 10.3760/cma.j.issn.0253-2727.2021.11.002.
中华医学会血液学分会实验诊断学组, 中华医学会血液学分会浆细胞疾病学组. 多发性骨髓瘤应用二代测序监测微小残留病的实验室标准化技术规范专家共识(2021年版) [J] . 中华血液学杂志, 2021, 42(12) : 974-977. DOI: 10.3760/cma.j.issn.0253-2727.2021.12.002.