



前言
随着国务院办公厅42号文发布,国家药品监督管理局药品审评中心于2021年底正式发布《以临床价值为导向的抗肿瘤药物临床研发指导原则》,临床试验设计将从界限分明的一期剂量爬坡看安全性,二期评估临床有效性,三期扩大的有效性试验的模式发生较大的整体转变。早期临床试验灵活的设计模式以期有效地加快抗肿瘤药物的临床开发,达到及早满足肿瘤患者对有效治疗需求的目的。随着政策落地,早期临床试验特别是一期临床试验对于药效学分析检测的需求将不断的提升,在一期验证安全性的同时进行药效学分析是临床快速向二期推进的关键指标。早期临床的药效学评估检测方法相对体外或者临床前的检测方法难度非常大,受到样品的基质复杂性,样品稳定性,个体差异等多方面因素的影响。本文Claudin18.2靶点抗体药物为例,简述下适用于临床阶段药效学评估,基于人免疫细胞的ADCC功能分析方法。
Claudin18.2药物研发进展
2016年ASCO年会上由Ganymed公司第一次公布了IMAB362(Zolbetuximab)的临床数据。IMAB362在Claudin18.2阳性的晚期胃癌及胃食管交界处癌惊艳的临床数据,让Claudin18.2靶点一跃成为国内快速跟进的热门靶点。至今的5年的时间里Zolbetuximab已在全球多中心开展Ⅲ期临床试验,国内Claudin18.2的抗体药物也在快速推进临床,部分Claudin18.2药物的信息如下。整体来说靶向Claudin18.2的药物呈现百舸争流,千帆竞渡的壮观场面,笔者认为在早期临床试验灵活的设计模式是快速推进靶向Claudin18.2的药物临床进展的关键因素,而临床阶段药效学评估是发挥临床试验灵活的设计模式不可或缺的一部分。
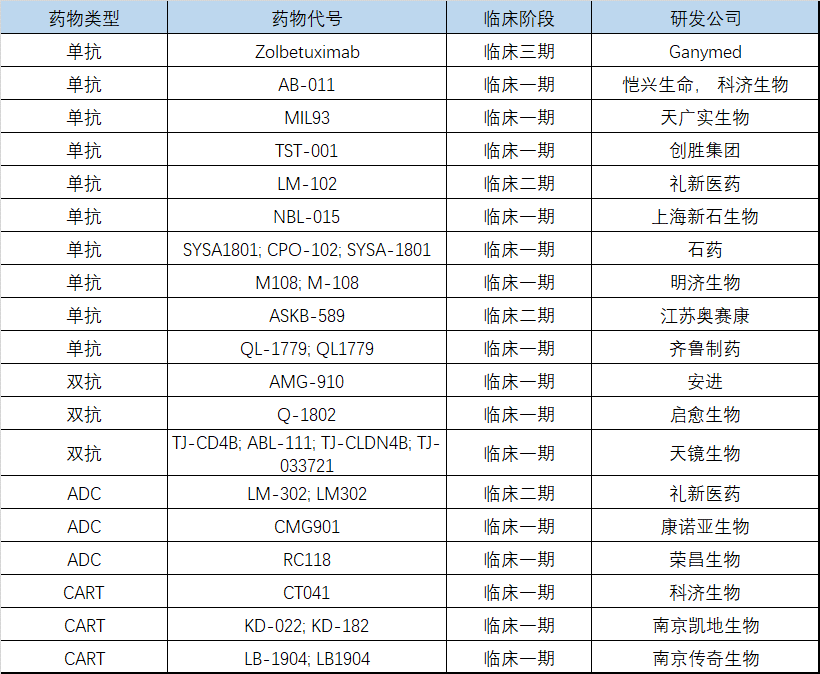
表1:部分Claudin18.2药物的研发进展
Claudin18.2抗体药物IMAB362 (Zolbetuximab)药效学分析方法分析解析
Zolbetuximab作为第一个进入临床靶向Claudin18.2的抗体药物,也是临床阶段推进最快的抗体药物,对于其药效学分析方法和数据,可以通过专利检索和文献得到,可作为靶向Claudin18.2候选在研药物的参考。本文主要通过已授权的专利文件US10421817B1和文献A phase I dose-escalation study of IMAB362 (Zolbetuximab) in patients with advanced gastric and gastro-oesophageal junction cancer记录的相关分析方法和数据,解析下临床阶段和临床前药效学评估方法的特征。
Zolbetuximab发挥药效学主要依赖的是其ADCC功能及CDC功能,关于ADCC功能从专利的描述临床前方法(图1)和文献记载的临床阶段(图2),方法条件参数的主要对比如表2
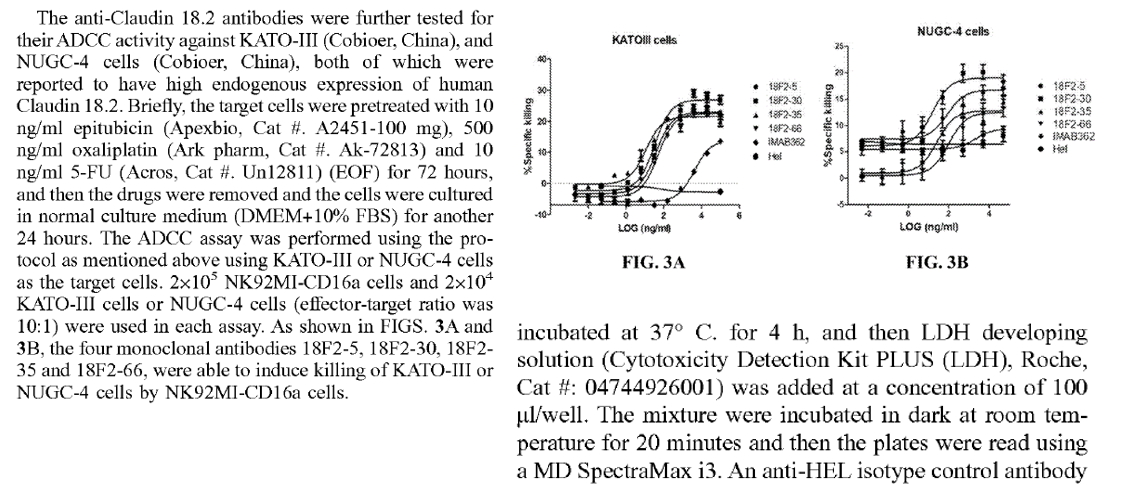
图1:专利描述的临床前药效评估方法
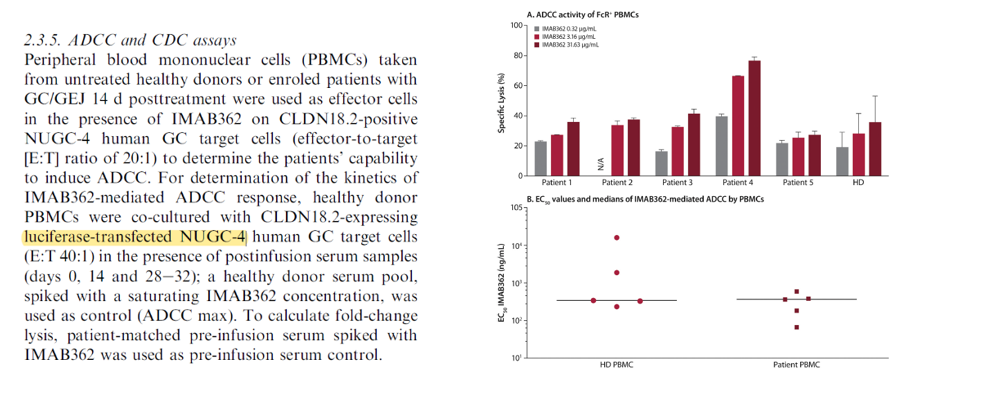
图2:文献描述的临床药效评估方法
表2:临床前和临床分析方法主要条件参数对比
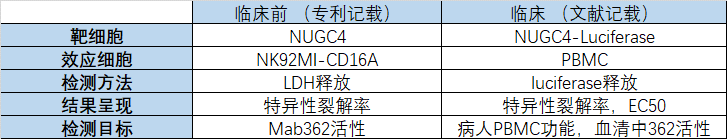
从条件参数对比来看,临床前和临床阶段的药效学评估方法可以说是两个完全不同的方法。从笔者较为丰富的临床药效学评估经验来看,之所以有这样的转换是基于临床检测的复杂性需要更加稳固和更加生理相关性的方法来达到临床检测的需求。如下图3,笔者归纳的常用的几种ADCC的检测方法中,Zolbetuximab文献记载的细胞杀伤的临床检测方法是更优的选择。
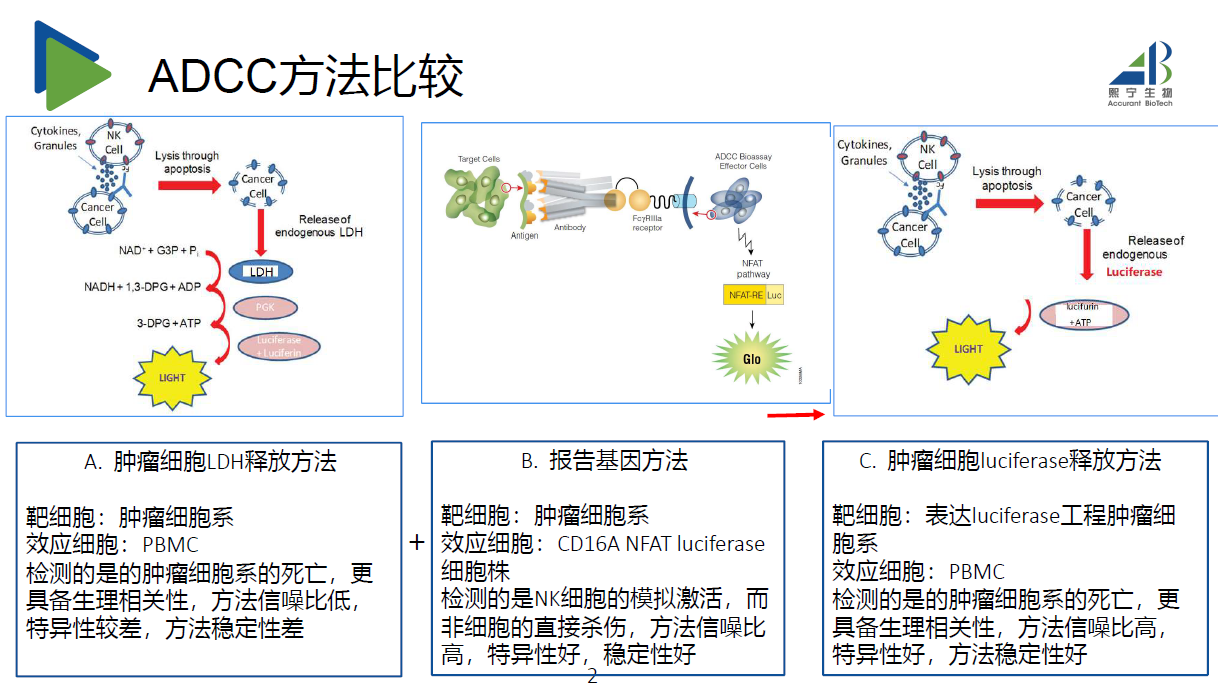
图3:主要的ADCC检测方法对比分析
熙宁生物自主开发的基于人免疫细胞的ADCC功能测定方法
熙宁生物基于Zolbetuximab披露的临床检测方法从NUGC4 CMV-luciferase稳转细胞株构建开始,自主开发了能够适用于临床阶段PBMC样品或者人血清Zolbetuximab样品的检测体系,适合靶向Claudin18.2的单抗,双抗和ADC药物的临床阶段样品分析的细胞杀伤药效学方法,有30倍以上更优的信噪比,复孔信号CV较小,方法稳固。
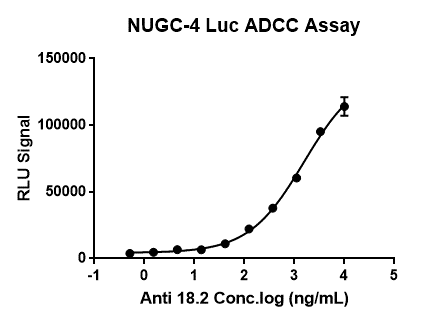
图4:熙宁生物自主开发的基于人免疫细胞的ADCC细胞杀伤方法
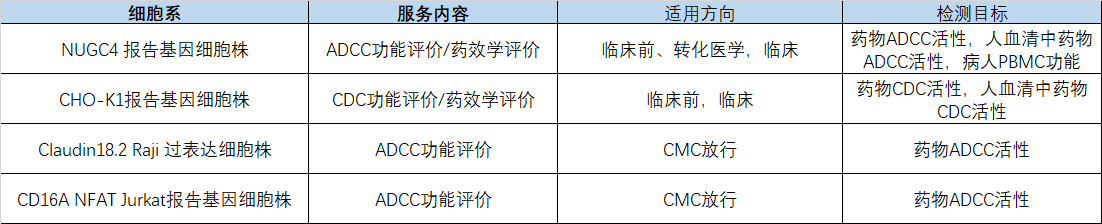
基于熙宁生物对于Claudin18.2抗体ADCC功能和细胞杀伤功能的深入研究,熙宁生物构建了基于人免疫细胞PBMC杀伤NUGC4 CMV-luciferase的检测方法,基于人免疫细胞PBMC使用人血清中的Claudin18.2抗体杀伤NUGC4 CMV-luciferase的检测方法; 基于人血清CDC功能杀伤CHO-K1 CMV-luciferase的方法等。可进行临床前和Zolbetuximab的药效学对比评估,临床阶段Claudin18.2相关药物的药效学评估,适用于CMC放行的Claudin18.2抗体 ADCC报告基因体系方法等,部分可出售的功能细胞系和检测服务如下表:
表3:熙宁生物Claudin18.2靶点的可出售稳转细胞系和检测服务内容
总结讨论
临床的药效学评估需要基于药物作用的理解,case by case的去设计临床阶段的样品分析方法,且该方法需要使用类似于临床样品的模拟样品来进行较为严格的方法学验证后才能用于临床样品的分析。通常情况下药效学评估没有明确的指导原则作为参考,以Fit to purpose为原则,验证参数也需要基于对于方法的理解和样品的基质环境,采集环境的了解进行设定。由于人样品基质环境的复杂性,个体药物作用的环境的差异性,不同采集时间样品的稳定性等因素的影响,药物的临床前的药效学分析方法往往不适用于临床样品分析,强行转换最大的可能性是得不到预期甚至前后矛盾的检测结果。
每一个药效学临床阶段的检测方法均是个性化定制的方法,方法的适用性,方法的稳健性,方法精密度等验证参数均没有固定的标准,需要CRO和药企相关负责人进行充分的信息共通基础上基于方法学开发的结果,方法学验证的参数和预期样品采集情况等去一步一步进行推进确定,紧密的沟通是开发一个合适的临床阶段药效学分析方法基础,高度专业化的技术能力是前提,严谨的方法学验证过程是得到一个稳健的临床阶段药效学分析方法的关键。