



DLL3靶点简介:DLL3 是Delta样配体(Delta-like ligands,DLLs)家族成员之一,一种抑制 Notch 信号的配体蛋白,附着于细胞表面的单次跨膜蛋白,属于 Notch 配体家族。人类 DLL3 基因位于 19q13 染色体上,DLL3蛋白由 619 个氨基酸组成,包括Delta/Serrate/LAG-2 (DSL) 结构域、六个表皮生长因子 (EGF) 样重复序列和一个跨膜结构域,其中较为保守的DSL结构域是与Notch受体结合的必要结构[1]。

图1 DLL3及其家族蛋白结构示意图[1]
PART 01
DLL3蛋白表达
DLL3蛋白在多种神经内分泌肿瘤(Neuroendocrine Neoplasms,NEN)中过表达。DLL3高表达常见于高级别神经内分泌肿瘤,而在低级别、分化良好的神经内分泌瘤(Neuroendocrine Tumor,NET)中DLL3表达较少[2]。

图2 DLL3在不同组织中的表达[2]

小细胞肺癌(SCLC)
小细胞肺癌(SCLC)是一种侵袭性、高级别的神经内分泌癌(Neuroendocrine carcinoma,NEC),恶性程度高,生存结果较差。DLL3在 SCLC 中的表达已得到广泛研究,DLL3在正常肺组织中不表达,在约80%以上的小细胞肺癌上高表达且定位于细胞质和/或细胞膜。大多数广泛期 SCLC 患者均观察到 DLL3 表达。研究表明[2], DLL3高表达的患者预后不良,中位总生存期明显短于低表达的的患者。

肺大细胞神经内分泌癌(LCNEC)
肺大细胞神经内分泌癌(LCNEC)与DLL3高 表达相关。在 LCNEC 患者中,26/70 (37.1%) 为 DLL3 阳性。较高比例 (75%) 的 IV 期 LCNEC 显示 DLL3 表达,其中大多数为细胞质表达[2]。

前列腺癌(CRPC-NE)
DLL3 在大多数去势抵抗性神经内分泌前列腺癌(CRPC-NE)(47 例中的 36 例,76.6%)和一部分去势抵抗性前列腺腺癌(56 例中的 7 例,12.5%)中都有表达,在局限性前列腺癌(194 例中的 1 例)和良性前列腺(103 例中的 0 例)中的表达极少或没有表达[3]。

胃肠胰神经内分泌肿瘤(GEP-NEN)
胃肠胰神经内分泌肿瘤 (GEP-NEN) 是一种罕见且异质性的肿瘤亚群。76.9% 的低分化NEC(G3 NEC)中存在 DLL3表达,而5 个具有高级别特征的分化良好的 GEP-NET(G3 NET)中没有 DLL3 表达,这表明 DLL3 表达是 G3 NEC 的标志物(p = 0.007)[4]。
PART 02
DLL3相关药物及IHC检测
针对DLL3靶点的药物类型有ADC、双抗、细胞治疗等,DLL3免疫组化检测在药物的临床开发进展中起到了比较重要的作用。

Rova-T
Rova-T(Rovalpituzumab tesirine)是第一个进入临床试验的DLL3靶点ADC药物[5]。经过一系列的临床试验,该药物还是失败了。IHC伴随诊断检测也很早就应用到了该药物的临床研究中,但是鉴于其临床试验设计及药物自身设计所暴露的问题,尤其是安全性方面,最终没能避开在Ⅲ期临床阶段折戟沉沙的命运[6]。这也为后续的ADC药物设计及药物临床试验安排提供了一个反面案例。
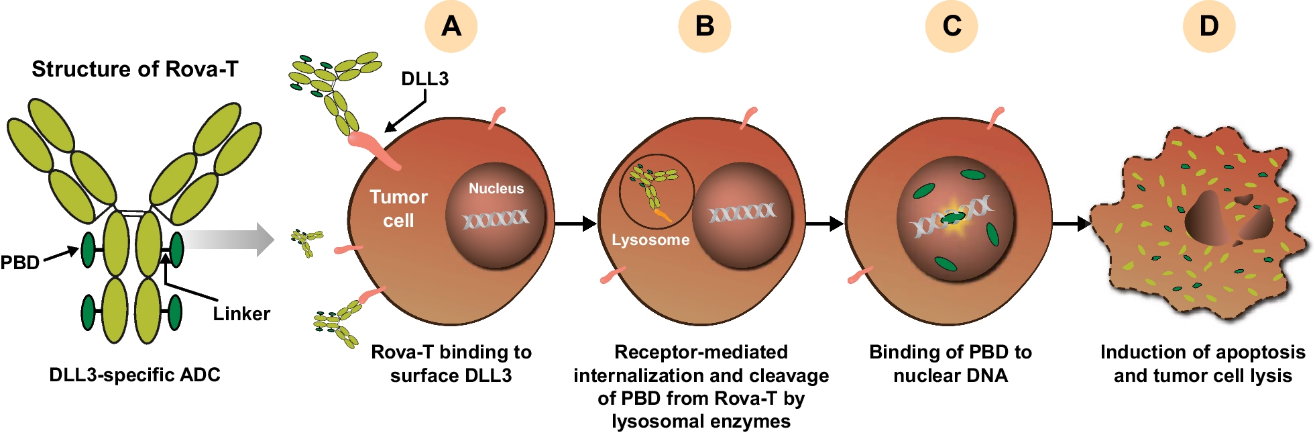
图3 Rova-T作用机制[5]

图4 Rova-T在广泛期SCLC的临床试验[6]

塔拉妥单抗(Tarlatamab)
安进公司的塔拉妥单抗(Tarlatamab)是一种新型双特异性T细胞衔接器(BiTE),靶向DLL3和CD3。2024年5月,FDA加速批准其用于治疗在铂类化疗后疾病进展的广泛期小细胞肺癌(ES-SCLC)。本次批准主要是基于一项开放标签、多中心、多队列的II期研究DeLLphi-301,该研究旨在评估塔拉塔单抗对既往接受过两种或两种以上疗法的晚期小细胞肺癌患者的抗肿瘤活性、安全性、副作用和药代动力学。
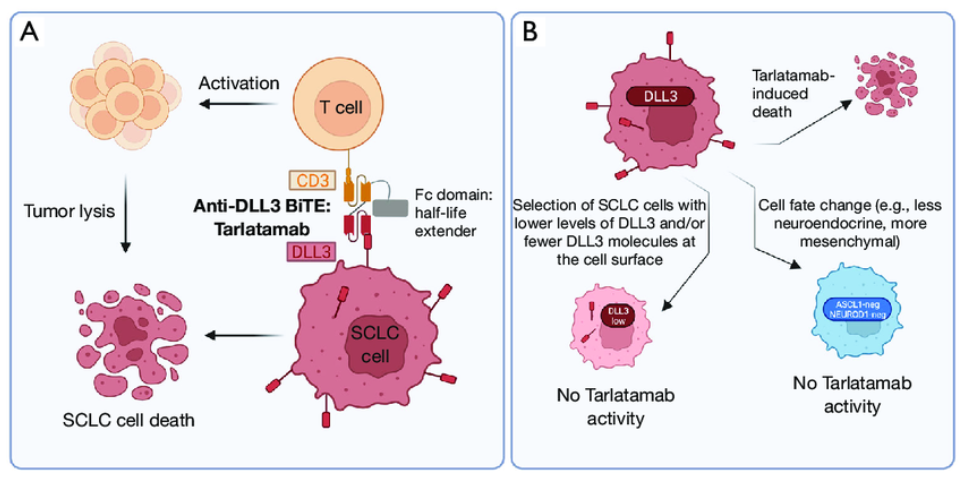
图5 塔拉妥单抗作用机制[7]
在 157 名 (84%) 拥有可评估肿瘤组织样本的患者中(10 mg组 83 名患者 [83%],100 mg组 74 名患者 [84%]),151 名 (96%) 的样本 DLL3 检测呈阳性。在DLL3 表达阳性患者、DLL3 表达阴性患者和没有可评估样本的患者中均观察到了客观反应[8](如下表所示)。可见DLL3的高表达可能起到了很重要的作用。但是该研究未见披露DLL3表达高低与药效的相关性数据,或许在未来的三期临床中能看到相关结果。
表1 塔拉塔单抗在肿瘤人群的治疗反应[8]


ZL-1310
宜联/再鼎的ZL-1310 是一款靶向DLL3的ADC药物。2024年10月24日再鼎公布了Ⅰ期药效结果,其中不表达 DLL3 的患者未观察到肿瘤缓解,H score大于5的患者都表现出了肿瘤缓解。至少接受过一次治疗后评估的患者的 ORR 为 74% (95%CI, 48.8, 90.9)。ZL-1310 的抗肿瘤活性在所有剂量水平上均得到证实。可见,该ADC药物也展现了不俗的疗效,期待未来有更大的进展。
以上3个临床试验充分说明,DLL3的免疫组化检测在靶向DLL3的药物临床中一直都是探索的热点方向。通过DLL3免疫组化检测可以很好地获得患者肿瘤组织DLL3的表达水平,进而对肿瘤患者进行分组,获得不同表达水平患者的药效结果,从而增大临床试验成功的概率。
PART 03
熙宁生物|精翰生物DLL3免疫组化检测服务
熙宁|精翰生物紧跟最新药物研发需求,致力于为申办方提供全面的DLL3表达检测方案,组织病理实验室已经建立了多种DLL3免疫组化检测方法,可快速响应申办方DLL3靶点药物临床试验检测需求。
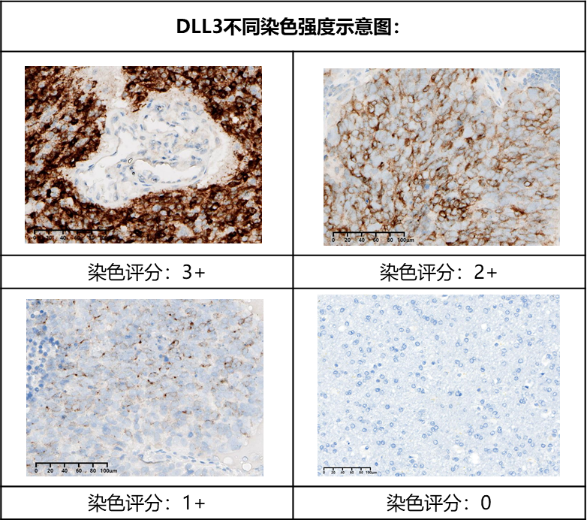
图6 DLL3染色强度示意图

图7 DLL3在不同癌种上的表达情况
熙宁生物|精翰生物病理实验室配备了一系列先进的仪器设备,包括Dako Autostainer Link48、Roche Benchmark Ultra、Leica Bond III 、Leica Bond Rx、Akoya PhenoImager™ HT全光谱玻片扫描仪、Halo多功能分析软件等,拥有一支强大的病理医生团队,可支持多种染色技术,如HE染色、免疫组化(单染、双染)、mIHC、RNAScope、FISH和特殊染色等,严格遵从CAP和GCP质量体系要求,可满足申办方临床试验阶段的入组筛查、生物标志物探索性研究、伴随诊断产品开发等多种需求。熙宁生物|精翰生物病理实验室目前已建立了超过200种免疫组化方法,开展超过100多个临床项目。未来,熙宁组织病理实验室将继续坚持高质量、高标准的服务理念,致力于为申办方提供技术过硬、质量可靠的产品服务。
欢迎后台留言咨询。

参考文献:
[1] Steinbuck MP, Winandy S. A Review of Notch Processing With New Insights Into Ligand-Independent Notch Signaling in T-Cells. Front Immunol. 2018;9:1230. Published 2018 Jun 1.
[2] Yao J, Bergsland E, Aggarwal R, et al. DLL3 as an Emerging Target for the Treatment of Neuroendocrine Neoplasms. Oncologist. 2022;27(11):940-951.
[3] Puca L, Gavyert K, Sailer V, et al. Delta-like protein 3 expression and therapeutic targeting in neuroendocrine prostate cancer. Sci Transl Med. 2019;11(484):eaav0891.
[4] Liverani C, Bongiovanni A, Mercatali L, et al. Diagnostic and Predictive Role of DLL3 Expression in Gastroenteropancreatic Neuroendocrine Neoplasms. Endocr Pathol. 2021;32(2):309-317.
[5] Rudin CM, Reck M, Johnson ML, et al. Emerging therapies targeting the delta-like ligand 3 (DLL3) in small cell lung cancer. J Hematol Oncol. 2023;16(1):66. Published 2023 Jun 24.
[6] Uprety D, Remon J, Adjei AA. All That Glitters Is Not Gold: The Story of Rovalpituzumab Tesirine in SCLC. J Thorac Oncol. 2021;16(9):1429-1433.
[7] Apaydin AA, Sage J. Taking it up a notch: a promising immunotherapy against small cell lung cancer. Transl Lung Cancer Res. 2023;12(5):948-952.
[8] Ahn MJ, Cho BC, Felip E, et al. Tarlatamab for Patients with Previously Treated Small-Cell Lung Cancer. N Engl J Med. 2023;389(22):2063-2075.