



前言
2022年9月9日,FDA批准TYK2抑制剂氘可来昔替尼(deucravacitinib)上市,用于治疗成年人中度到重度斑块状银屑病,成为近10年来全球首款获批上市的中度至重度斑块状银屑病口服治疗药物。Deucravacitinib同时在欧洲药品管理局和日本厚生劳动省获得了上市受理,其用于申报的三期临床研究随机入组 220 名中重度斑块状银屑病亚洲(中国大陆、中国台湾和韩国)患者,其中 180 名为中国人群,占比超 80%,因此在中国申报上市估计也不太远了。BMS的Deucravacitinib在全球多个主要市场同步申报上市,足见BMS对于该药物的信心,相信Deucravacitinib后续会拓展更多自身免疫适应症,市场潜力巨大。本文通过调研BMS-986165的早期药效学生物标志物检测文献资料,来浅析该药效学方法的难点,并借此案例阐述在临床Ⅰ期进行早期药效学生物标志物检测的作用和价值。
TYK2抑制剂药物的研发进展
随着BMS的deucravacitinib在成年人中度到重度斑块状银屑病临床试验中取得极大的成功,相较于同家族的JAK抑制剂,TYK2特异性抑制剂的临床获益正逐渐显现,但目前所知,该管线的研发企业并不多,部分研发企业如下:
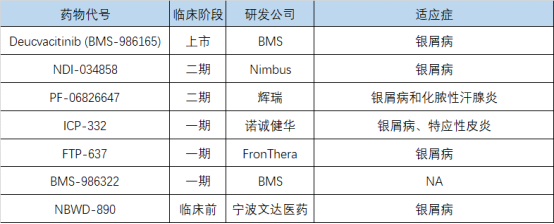
TYK2抑制剂临床药效学生物标志物的检测方法解析
Deucravacitinib是一款口服高选择性酪氨酸激酶2(TYK2)变构抑制剂。TYK2是一种细胞内信号激酶,介导白细胞介素IL-23、IL-12、I型干扰素(IFN)的信号传导,这些细胞因子是参与炎症和免疫反应的天然细胞因子。Deucravacitinib通过选择性与TYK2蛋白调控结构域结合,使TYK2处于失活状态,从而特异性抑制TYK2的活性,不影响蛋白JAK1、JAK2或JAK3,进而避免相关心血管事件或静脉血栓栓塞不良事件的发生。
基于文献简要描述,Deucravacitinib临床药理学的检测方法需要使用IL12/IL18刺激用药前后的全血,通过检测刺激后全血中的IFNγ水平来表征Deucravacitinib(BMS-986165)的药效,根据熙宁实验室的实战经验,该分析方法有以下难点:
1.全血基质中的细胞成分复杂,刺激效果可能会受到影响,IL12/IL18刺激全血的条件需要进行摸索。
2.IL12为异源二聚体,不同细胞因子供应商重组表达出来IL12的活性差异较大,需要进行筛选。
3.全血的稳定性较差,在临床采样运输过程中需要充分评估全血保藏稳定性对样品检测的影响。
4.需要根据药物的PK数据优化全血刺激检测IFNγ的检测模型,确保方法学的灵敏度能够满足检测的需求。

熙宁生物自主开发的TYK2抑制剂药理学分析方法
熙宁生物有丰富的临床药理分析经验,基于TYK2抑制剂自主开发了临床药理学分析方法,具备丰富的实战经验,欢迎咨询。部分经验分享如下图:
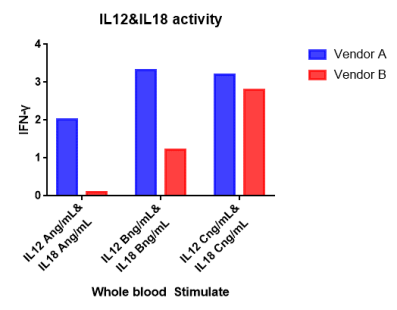
IL12/IL18细胞因子筛选
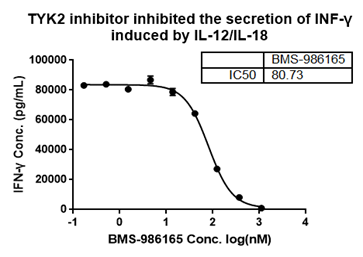
BMS-986165在全血刺激模型中的剂量曲线